Батарейки и элементы питания. Принцип действия
Сложно представить современную жизнь без батареек. Они есть везде и получили широкое распространение, поскольку дают нам с вами возможность брать с собой энергию. И пусть, как правило, это не долговечный источник питания, но он способен нам с вами существенно упростить жизнь. Посудите сами, если бы не было бы батареек, приходилось бы включать и выключать телевизор, вставая с кровати. В отсутствии таких элементов питания, не было бы веселых детских игрушек портативных плееров. Со времён своего появления батарейки настолько эволюционировали, что появились аккумуляторы. Благодаря последним стало возможно включать зажигание автомобиля без механического раскручивания стартера. Также, благодаря им стало возможно производство мобильных телефонов, смартфонов и планшетов, без которых ни один современный человек не обходится. Давайте сегодня поговорим про батарейки, их принцип действия и начнем мы с истории.
Изобретателем, и человеком, который построил первую работающую батарейку принято считать Алессандро Вольта.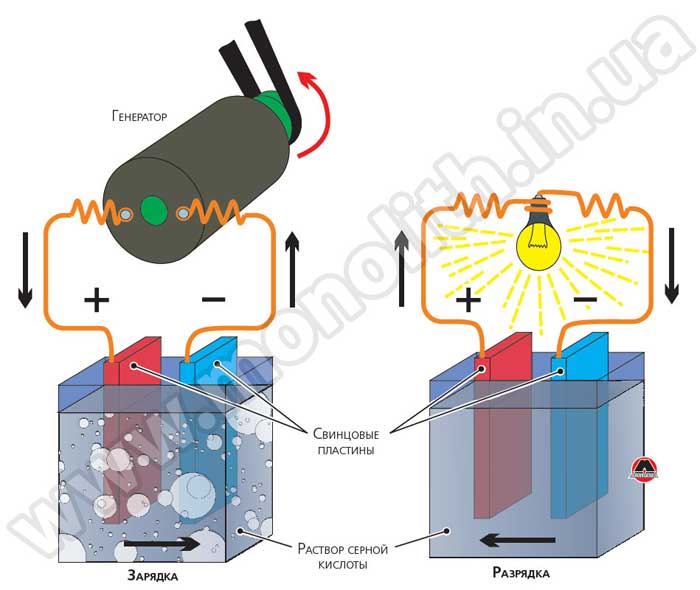
Современные батарейки ушли далеко вперёд. Они способны выдавать гораздо больше энергии и более длительное время, при меньших размерах. Батарейкой в обиходе, как правило называют одиночный гальванический элемент. Хотя это не совсем правильно. Батарея или батарейка — это последовательное соединение нескольких гальванических элементов. Типичным примером батарей является автомобильный аккумулятор, который в зависимости от потребностей машины состоит из шести или двенадцати гальванических элементов.
Катод и анод в батарейке находится в виде пасты. Катодную массу прессуют изнутри к внешнему корпусу батарейки. В середине находится анод, из которого выходит латунный сердечник. Последний соединяет анодную пасту с дном батарейки. Важно! Анодная паста не соединяется с плюсом батарейки. Для того, чтобы анодная и катодная пасты не смешивались, между ними кладут нетканый материал, вымоченный в электролите.
Давайте коротко поговорим об аккумуляторных батареях. Они бывают разными по своему составу. Разница между аккумулятором и батарейкой в том, что в аккумуляторе при разрядке происходят обратные реакции. Проще всего это объяснить на примере автомобильного свинцового аккумулятора. При разрядке такого аккумулятора на катоде происходит восстановление диоксида свинца. На аноде в этот момент происходит окисление свинца. Обе эти реакции обратимые, и при зарядке происходит совершенно противоположный процесс. Так устроены все аккумуляторы, вопрос только в размерах, составе и конструкции. Но фундаментальная суть, повторяюсь одна, все аккумуляторы построены на обратимых реакциях. Например, аккумулятор мобильного телефона использует тот же принцип, но в нем содержится литий вместо свинца.
На аноде в этот момент происходит окисление свинца. Обе эти реакции обратимые, и при зарядке происходит совершенно противоположный процесс. Так устроены все аккумуляторы, вопрос только в размерах, составе и конструкции. Но фундаментальная суть, повторяюсь одна, все аккумуляторы построены на обратимых реакциях. Например, аккумулятор мобильного телефона использует тот же принцип, но в нем содержится литий вместо свинца.
Существует так же литиевые одноразовые батарейки. Они стоят достаточно дорого, но у них есть масса плюсов. Во-первых, они обладают максимальной мощностью на единицу веса. Во-вторых, они работают гораздо дольше, нежели солевые или щелочные батарейки. В-третьих, литиевые батарейки имеют гораздо больший срок годности. Он составляет от десяти до двенадцати лет, в тот момент, как щелочные могут храниться только 5‒7 лет. Литиевые батарейки имеют схожую с щелочными конструкцию. Так что подробно на ней останавливаться не будем.
Последнее, о чем успеем поговорить сегодня — сахарные батареи. На данный момент — это лишь разработка, никакого практического применения она пока не имеет, хотя довольно успешно проходила испытания. Принцип такой батареи заключается в реакции полисахаридов, полученных из крахмала с уксусом. Конечно, это очень грубое описание происходящего в батарее, но зато понятное. В такой батарее самая высокая плотность энергии. К тому же, такие батарейки, как правило имеют возможность перезарядки, а значит из можно использовать достаточно долго. Но самая классная фишка сахарных аккумуляторов и батарей в другом, они полностью биоразлагаемы. Это значит, что такие батареи, в отличии от щелочных можно просто выкидывать, они не угрожают окружающей среде.
На данный момент — это лишь разработка, никакого практического применения она пока не имеет, хотя довольно успешно проходила испытания. Принцип такой батареи заключается в реакции полисахаридов, полученных из крахмала с уксусом. Конечно, это очень грубое описание происходящего в батарее, но зато понятное. В такой батарее самая высокая плотность энергии. К тому же, такие батарейки, как правило имеют возможность перезарядки, а значит из можно использовать достаточно долго. Но самая классная фишка сахарных аккумуляторов и батарей в другом, они полностью биоразлагаемы. Это значит, что такие батареи, в отличии от щелочных можно просто выкидывать, они не угрожают окружающей среде.
Сегодня мы с вами поговорили о большом количестве разнообразных батареек и разобрались с их принципом действия. Но осталось несколько вопросов которые мы с вами не решили. Например, как подобрать правильные батарейки? Или какой формы выпуска они бывают? Так что ждём вас в следующий раз, на этом же месте в тоже время.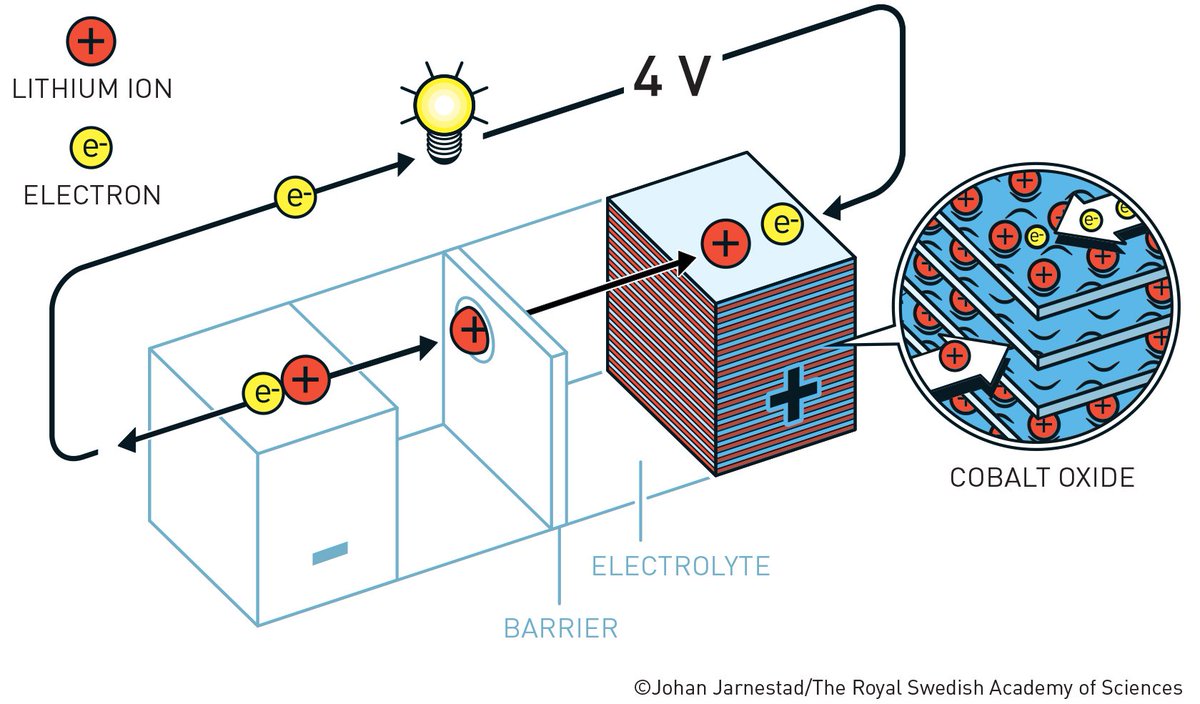
Как работают батарейки и аккумуляторы?
Где бы вы ни были и куда бы ни пошли, вы, так или иначе, столкнетесь с батарейками или аккумуляторами. Попробуйте представить мир, в котором бы все электроприборы питались от розеток – никаких телефонов, фонариков, ноутбуков, автомобилей и прочих уже привычных благ цивилизации. Аккумуляторы повсюду: от мобильных телефонов до космических кораблей. О том, как работают эти портативные источники энергии, из чего они сделаны, и какие мифы о них правдивы, а какие – нет, мы попытаемся разобраться в этой статье.
Первые батарейки
Считается, что примитивными батарейками пользовались еще арабы во времена до нашей эры. В результате раскопок под Багдадом археологи нашли глиняные кувшины, в которых находились железные стержни в медной оболочке. Протестировав находки в лаборатории, ученые пришли к выводу, что кувшины были наполнены кислотной жидкостью, скорее всего, вином или уксусом.
Первый в истории стабильный химический источник питания. Автор: dpantalony
Однако первые современные батарейки появились в 1800 году благодаря итальянскому ученому Алессандро Вольте, который получил непрерывный электрический ток, поместив цинковые и медные пластины в кислоту. Это изобретение получило название Вольтов столб, а единица измерения напряжения получила название в честь его создателя. С тех пор появились новые виды батареек с усовершенствованной конструкцией и улучшенным коэффициентом полезного действия, но принцип их работы существенно не изменился: при подключении батарейки к устройству в ней происходит электрохимическая реакция и вырабатывается электричество.
По типу электрохимической реакции различают два типа химических источников питания:
1.
2. Аккумуляторы. Они отличаются обратимостью реакций при выработке электричества, поэтому их можно перезарядить. Аккумуляторы могут не только, как батарейки, преобразовывать химическую энергию в электрическую, но и наоборот.
Как работают батарейки
Оригинал: Microsoft Encarta
Главными компонентами батарейки, из которых она состоит на 90 %, являются электролит и два электрода: анод
 Во время работы батарейки в аноде (-) вырабатывается избыточное количество электронов, и единственным выходом для них является перемещение к положительному полюсу. Взаимодействуя с материалом катода, электроны нейтрализуются в результате реакции восстановления. Именно избыток электронов в отрицательном полюсе и их нехватка в положительном полюсе приводит к постоянному перераспределению электронов между полюсами и создает электрическое напряжение. Окислительно-восстановительные процессы протекают в батарейке постоянно, пока она подключена к электрической цепи, изменяя изначальный состав материалов анода и катода: образуются второстепенные элементы, которые препятствуют движению электронов. Это приводит батарейку в негодность.
Во время работы батарейки в аноде (-) вырабатывается избыточное количество электронов, и единственным выходом для них является перемещение к положительному полюсу. Взаимодействуя с материалом катода, электроны нейтрализуются в результате реакции восстановления. Именно избыток электронов в отрицательном полюсе и их нехватка в положительном полюсе приводит к постоянному перераспределению электронов между полюсами и создает электрическое напряжение. Окислительно-восстановительные процессы протекают в батарейке постоянно, пока она подключена к электрической цепи, изменяя изначальный состав материалов анода и катода: образуются второстепенные элементы, которые препятствуют движению электронов. Это приводит батарейку в негодность.Аккумуляторы
Аккумуляторы отличаются от батареек обратимостью химических процессов, проще говоря, возможностью перезарядки. В электрической цепи аккумулятор работает так же, как и батарейка: в аноде образуются электроны, которые перемещаются в катод, образуя электрическое напряжение. Когда материал анода истощается, электроны прекращают вырабатываться и аккумулятор садится. Вот здесь и кроется главное преимущество аккумуляторы: в отличие от батарейки, анод можно восстановить, пропустив через аккумулятор электрический ток. Естественно, это не значит, что аккумуляторы будут работать вечно, ведь материал анода в любом случае будет постепенно истощаться, но на сотню перезарядок обычного аккумулятора зачастую хватает.
Когда материал анода истощается, электроны прекращают вырабатываться и аккумулятор садится. Вот здесь и кроется главное преимущество аккумуляторы: в отличие от батарейки, анод можно восстановить, пропустив через аккумулятор электрический ток. Естественно, это не значит, что аккумуляторы будут работать вечно, ведь материал анода в любом случае будет постепенно истощаться, но на сотню перезарядок обычного аккумулятора зачастую хватает.
В зависимости от материалов, используемых в качестве анода и катода, выделяют разные типы батареек. Каждый тип отличается производительностью, сроком эксплуатации, ценой и вредностью. К сожалению, не существует идеальных батареек, которые бы удовлетворяли пользователей всеми параметрами. О типах батареек и аккумуляторов, их преимуществах и недостатках читайте далее.
Принцип работы типовой батарейки | БАТАРЕЙКУ.РФ
Батарейка, какой бы миниатюрной она не казалась, — это уменьшенная «электростанция», занятая преобразованием химических процессов в электроэнергию.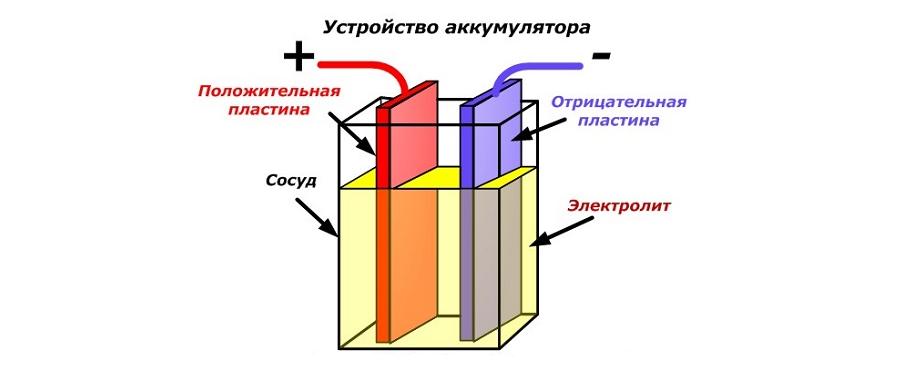
Различия, которые существуют между разными видами батареек, не так значительны, как факторы, их объединяющие.
И главным фактором, роднящим все типы элементов питания, является принцип их работы, о котором мы расскажем в очередной статье сайта http://www.батарейку.рф.
Принцип работы типовой (марганцево-цинковой) батарейки
1. Начало химических реакций
Химические процессы запускаются в элементах питания, как только те оказываются подключенными к замкнутой цепи.
Другими словами, батарейка начинает вырабатывать электроэнергию тогда, когда мы:
- вставляем ее в устройство — потребитель,
- включаем батарейку в работу,
- замыкаем контакт цепи.
С этого момента химические элементы, помещенные внутрь корпуса, вступают в реакцию, побочным результатом которой является выделение энергии: электрической и тепловой.
Разделительный элемент, входящий в состав батарейки, обеспечивает правильность текущих процессов, направляя энергию в нужное русло.
2. Суть реакции
- Измельченные частицы цинка анода окисляются электролитом.
- Катод (двуокись марганца + углерод) посредством реакции на окисленный цинк образует течение электронов.
- Вырабатываемое электричество захватывается токосъемником и подается на внешние контакты батарейки, обеспечивая ее полярность, питая внешние устройства энергопотребления (фонарик, часы, плеер и т.д.).
3. Падение напряжения
В результате внутренних реакций химические компоненты батарейки сокращаются (иссякают запасы двуокиси марганца).
Цинковый анод окисляется, двуокись марганца на катоде утрачивает потенциал, превращаясь в неизбежную помеху, отработанный материал.
Как следствие — падение напряжения в сети.
Со временем побочных продуктов реакции становится все больше, а поскольку корпус элемента питания закрыт, они начинают препятствовать нормальным процессам вырабатывания энергии.
Так происходит до тех пор, пока батарейка оказывается неспособной утолить потребности питающего устройства в напряжении.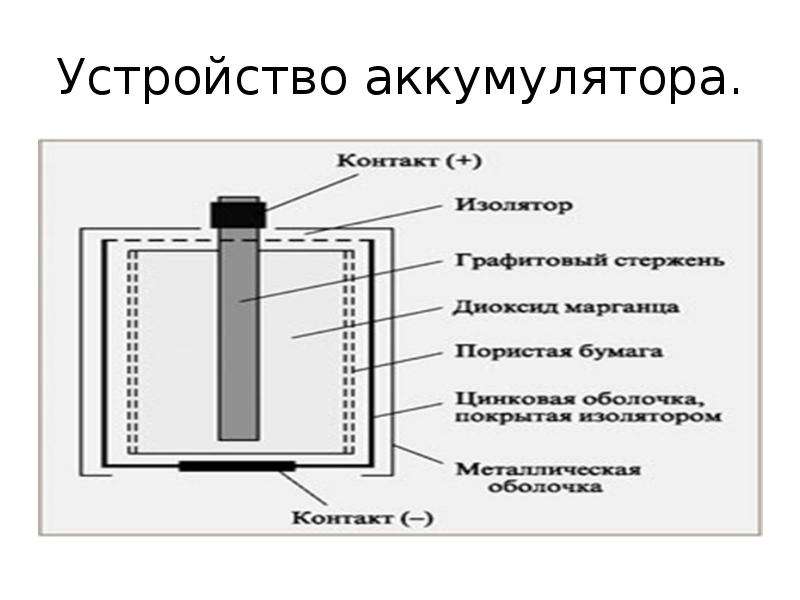
После чего одноразовая батарейка может быть сдана на утилизацию.
Что такое батарейка? Состав батарейки
В электротехнике термином батарейка называют некий источник электрического тока в котором несколько электрохимических элементов соединёны между собой. Электричество в батарейке вырабатывается под действием химического процесса. Обратите внимание, что именно «несколько», а не одиночный элемент называется батарейкой. Но, всё же, мы привыкли батарейкой называть всё, что даёт нам постоянный ток, не вникая в то, из чего она там внутри состоит. Тем более, что как правило, снаружи всё упаковано в единую форму.
Изобретателем батарейки считается итальянский физик Алессандро Вольта. И произошло это примерно в 1800 году.
Принцип работы батарейки
У любой батарейки есть анод (положительный полюс, обозначается значком +), катод (отрицательный полюс, обозначается, соответственно значком -), между ними электролит (как правило сухой).
Электрический ток бежит от анода (-) к катоду (+), но между ними обязательно должна быть нагрузка (например лампочка или, что-то ещё).
Если нет нагрузки — нет тока!
А если соединить полюса в батарейке без нагрузки, то произойдёт короткое замыкание.
Качество батарейки (мощность, продолжительность работы, параметры нагрузки..) зависят от состава и качества материалов в её составе.
Виды батареек
Классификация батареек по типу химической реакции
| Тип | Описание | Достоинства | Недостатки |
| Первичные | Гальванические элементы. Реакции, происходящие в них, необратимы, поэтому их нельзя перезарядить. | Дешевле стоят, меньше саморазряд. | Одноразовые. |
| Вторичные | Аккумуляторы. Реакции в них обратимы, поэтому они способны не только отдавать энергию, но и накапливать её. Реакции в них обратимы, поэтому они способны не только отдавать энергию, но и накапливать её. |
Многократность применения. Более экологичные. | Дороже. Сильнее саморазряд. |
Классификация батареек по типу электролита
(список не полный, указаны только самые распространённые в быту)
| Тип | Достоинства | Недостатки | Фото |
|---|---|---|---|
| «Солевые» (угольно-цинковые) | Самый дешёвый. Рабочая температура: от −40 до +55 °C (данные Википедии). | Малая емкость, не позволяющая использовать изделия в мощных устройствах, малый срок хранения. | |
| «Щелочные» (алкалиновые, щёлочно-марганцевые) | Ёмкость в 1,5–10 раз больше, чем у солевых элементов, в зависимости от режима работы, при том же типоразмере элемента. Меньший саморазряд, длительный срок хранения. Лучше работают при больших токах нагрузки. Меньше падение напряжения по мере разряда. Меньше газовыделение, благодаря чему элемент можно делать полностью герметичным. Рабочая температура: от -30 до +55 °С. Меньший саморазряд, длительный срок хранения. Лучше работают при больших токах нагрузки. Меньше падение напряжения по мере разряда. Меньше газовыделение, благодаря чему элемент можно делать полностью герметичным. Рабочая температура: от -30 до +55 °С. |
Спадающая кривая разряда, большая масса. | |
| «Литиевые» | Наивысшая ёмкость на единицу массы. Пологая кривая разряда. Превосходен при низких и высоких температурах (лучше чем у предыдущих элементов). Длительное время хранения. Лёгкий вес. | Высокая цена |
Типы батареек по размеру и их обозначения
Здесь мы разместили таблицу в которой указаны, помимо размеров и характеристик, «название» и «маркировка». По сути это одно и то же, и даже, как правило, на всех элементах указывается одновременно. В США принято буквенное обозначение (в колонке «название»), и оно ориентированно на физический размер «батарейки».
| Название |
Фото | Маркировка |
Диаметр (мм) |
Высота (мм) |
Емкость (мАч) |
|---|---|---|---|---|---|
| A | Солевая (R23) Щелочная (LR23) |
17 | 50 | — | |
| AA | Солевая (R6) Щелочная (LR6) Литиевая (FR6) |
14,5 |
50,5 |
1100-3500 |
|
| AAA | Солевая (R6) Щелочная (LR6) Литиевая (FR6) |
10,5 | 44,5 | 540-1300 | |
| AAAA | Щелочная (LR8D425) |
8. 3 3 |
42.5 | 625 |
|
| B | Щелочная (LR12 или 3R12) |
22 | 62 × 67 | 8350 | |
| C | Солевая(R14)
Щелочная(LR14) |
26.2 | 50 | 3800-8000 | |
| D | Солевая(R20) Щелочная(LR20) |
34.2 | 61.5 | 8000-19500 |
|
| F | Солевая(R25) Щелочная(LR25) |
33 | 91 | — | |
| N | Солевая(R1) Щелочная(LR1) |
12 | 30.2 | 1000 | |
| 1/2AA | Солевая (R14250) |
14.5 | 25 | 250 |
* Параметры ёмкости и тока в батарейке могут отличаться в зависимости от производителя.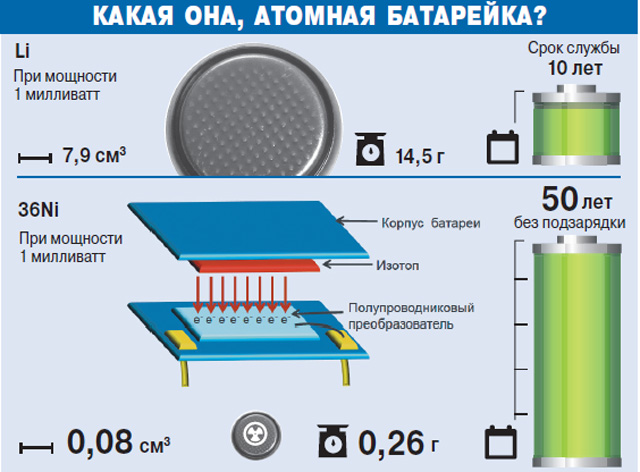
Маркировки батареек
Маркировку гальванических источников тока делают исходя из состава электролита и активного металла в их конструкции. Регламентирует всё это IEC (Международная электротехническая комиссия).
По этой классификации существует 5 самых распространенных типов круглых (цилиндрических) батареек:
солевые, щелочные, литиевые, серебряные и воздушно-цинковые.
Мы рассмотрим первые три, поскольку в предыдущей таблице не стали описывать стандарты для двух последних (серебряных и воздушно-цинковых батареек). Разнообразие этих элементов гораздо шире и мы не уместимся в рамки статьи.
Буква R в их маркировке означает круглую форму (от английского round).
Солевые батарейки (R).
Катод состоит из марганца (MnO2) в смеси с графитом (около 9,5 %), анод из цинка (Zn), и электролит из раствора хлорида аммония NH4Cl. Они обеспечивают напряжение 1,5 вольта, имеют небольшую емкость, высокий саморазряд и низкий срок хранения (примерно 2 года).
Солевые батарейки самые дешевые и имеют посредственные технические характеристики. В обиходе их также называют цинк-карбоновыми и угольно-цинковыми. Наиболее эффективной областью применения солевых батареек являются приборы со средним и низким энергопотреблением. Например, пульты ДУ и настенные часы.
Щелочные батарейки (LR).
Имеют катод из диоксида марганца, анод из цинка (порошок), и электролит из гидроксида щелочного металла (обычно гидроксид калия). Они имеют напряжение 1,5 вольта, увеличенную емкость, низкий саморазряд и большой срок хранения до 10 лет.
Эти источники тока несколько дороже солевых, в обиходе их еще называют алкалиновыми и щелочно-марганцевыми.
Литиевые батарейки (CR).
Имеют анод из лития, катод чаще из диоксида марганца (но используются и другие составы для катода). Они имеют большую емкость, малый саморазряд и большой срок хранения до 10-12 лет. Они сохраняют работоспособность при низких температурах. Эти источники тока довольно дороги.
Эти источники тока довольно дороги.
Надеемся, что вы нашли ответ на вопрос «что такое батарейка?».
Полезные статьи не только про батарейки
| Как выбрать часы | Ремонт часов | Замена батареек | Таблица сравнения батареек |
Воздушно-цинковые батарейки — типы и принцип работы
Воздушно-цинковые батарейки используются во всех современных цифровых слуховых аппаратах. Во время работы воздушно-цинковые элементы питания используют в качестве катода кислород, поглощаемый из воздуха, а в качестве анода — порошок цинка.
Как работают слуховые батарейки
Благодаря удалению из корпуса батарейки оксида ртути или серебра, которые до сих пор служили в качестве катода, в нем освободилось больше пространства для цинкового порошка. Поэтому воздушно-цинковые батарейки более энергоемкие, если сравнивать между собой батарейки разного типа. Ниже приведена сравнительная характеристика срока службы алкалиновой и воздушно-цинковой батареек. Как видно из рисунка воздушно-цинковая батарейка работает не только дольше, но и держит свое напряжение постоянным в течение всего срока эксплуатации. С воздушно-цинковой батарейкой Вы можете ожидать от своих слуховых аппаратов более чистого звучания, нормальной и стабильной работы всех его систем. И еще одним очень важным преимуществом является то, что они не текут, как скажем, щелочные батареи. На графике видно, что воздушно-цинковые элементы питания не только служат дольше, но и равномерно отдают свой заряд в течение всего срока службы в отличие от, скажем, щелочных батареек. Это значит, что Вам не придется постоянно прибавлять громкости, а слуховой аппарат будет обеспечен током необходимого напряжения для нормальной работы всех его функций на протяжении всей службы батарейки.
В состоянии хранения (храниться они могут 2 и более лет) воздушные отверстия батареек заклеены липкой пленкой. Как только Вы срываете защитную пленку с положительного контакта, батарея активируется и начинает отдавать энергию. Разряд активированной батарейки происходит независимо от того, питает она слуховой аппарат или просто лежит на столе. Поэтому срывать защитную пленку следует только, если Вы действительно будете использовать ее в слуховом аппарате.
Время работы батареек составляет от нескольких дней до нескольких недель. К концу периода работы Вашей батарейки Вы заметите, что слуховой аппарат стал работать заметно тише. Значит, пришло время заменить батарейку.
Если воздушно-цинковая батарейка разряжена почти полностью, то обычно заметны следующие проявления: после включения слуховой аппарат работает совершенно нормально, но через короткое время почти полностью замолкает. Чем более разряжена батарейка, тем быстрее замолкает слуховой аппарат.
Размеры батареек для слуховых аппаратов
В каталоге слуховых аппаратов представлено более 100 моделей аппаратов, которые отличаются по стилю, типу и размеру корпуса, уровню мощности и набору технологий. В связи с этим они потребляют разное количество энергии. Например, для мощных слуховых аппаратов потребуются элементы питания большей мощности и соответственно большего размера.
В настоящее время для слуховых аппаратов доступно 4 типоразмера батареек. Размеры от самых маленьких до самых больших: 10, 312, 13 и 675.
Типоразмер №10 — диаметр 5,8 мм, высота -3,6 мм
Типоразмер №312 — диаметр 7,9 мм, высота 3,6 мм.
Типоразмер №13 — диаметр 7,9 мм, высота 5,4 мм.
Типоразмер №675 — диаметр 11,6 мм высота 5,4 мм.
Цветная маркировка слуховых батареек
Типы слуховых батареек имеют незначительные отличия в размере, поэтому, чтобы упростить процесс покупки батареек для Ваших слуховых аппаратов, производители маркируют каждый размер элемента питания определенным цветом.
Типоразмер №13 — оранжевый
Типоразмер №10 — желтый
Типоразмер №312 — коричневый
Типоразмер №675 — синий.
Если у Вас возникли трудности с покупкой батареек для Ваших слуховых аппаратов, Вы всегда можете обратиться к специалистам Центра хорошего слуха, которые помогут определить нужный размер батареек и предложат на выбор батарейки для слуховых аппаратов от ведущих производителей элементов питания: Rayovac, Widex, ReSound, PowerOne.
Как правильно использовать и хранить слуховые батарейки
- Используйте слуховые батарейки типоразмера, указанного в паспорте или инструкции по эксплуатации к Вашим слуховым аппаратам.
- Для подготовки к работе необходимо удалить наклейку и дать время активному веществу насытиться кислородом (от 3 до 5 минут). Если начать эксплуатацию батарейки сразу после вскрытия, то активация произойдет только в поверхностном слое вещества, что существенно скажется на сроке службы.
- Каждый раз, вставляя батарейку, обращайте внимание на плюсовую сторону. Плюсовая сторона отличается тем, что является плоской и обычно имеет на себе одно или несколько воздушных отверстий и небольшой крестик — плюс в центре.
- Используйте батарейку до конца, после чего вставьте новую. Не храните уже использованные батарейки.
- Храните батарейки в блистерах при комнатной температуре и нормальной влажности. Желание «сберечь» подольше батарейки в холодильнике может привести к прямо противоположному результату — слуховой аппарат с новой батарейкой вообще не заработает.
- Выключайте слуховой аппарат, когда им не пользуетесь. На ночь вынимайте источники питания из аппарата и оставляйте открытым батарейный отсек.
- Всегда имейте при себе новую запасную батарейку. Запасные батарейки не должны храниться вместе с металлическими предметами (ключами, другими батарейками), которые могут закоротить контакты батарейки, и вызвать ее преждевременный разряд или порчу. Лучше поместить каждую запасную батарейку в индивидуальный изолирующий контейнер.
- Храните батарейки в местах, недоступных для детей. Дети могут проглотить батарейки и этим причинить вред здоровью.
Где купить батарейки для слуховых аппаратов
Приобрести батарейки для вашего слухового аппарата вы можете в ближайшем Центре хорошего слуха, а также заказать их доставку на сайте. Как официальный поставщик на территории Беларуси мы гарантируем высочайшее качество (без китайских подделок) и лучшие цены на элементы питания для ваших слуховых аппаратов.
Из-за больших объемов продаж мы регулярно пополняем запасы на складе, а вы всегда получаете только свежие батарейки.
Если вдруг вы забыли какой размер батарейки подходит для вашего слухового аппарата, специалисты Центра помогут вам купить батарейки правильного типоразмера.
Принцип работы батарейки — Как образуется ток?
Как работают настенные часы, пульт от телевизора или детская игрушка на радиоуправлении? Большинство людей, не задумываясь, ответят — «от батареек» и будут, в принципе, правы. Но вряд ли кто-то из них сможет рассказать, как именно портативный элемент питания утроен, каким образом он функционирует и без чего весь процесс передачи электрического тока от батарейки к конечному потребителю был бы невозможен. Давайте же восполним этот досадный пробел в знаниях.
Разделы статьи
Что такое батарейка
В батарейках электричество возникает благодаря взаимодействию разных химических веществ. И принцип работы этих изделий легко можно отыскать в учебниках по физике. Все элементы собраны из одних и тех же частей.
Устройство батарейки
Устройство батарейки простое. Различия между разными типами батарей минимальны. В основе каждой конструкции имеются:
- Полюс положительный — анод.
- Полюс отрицательный — катод.
- Электролит.
Как работает батарейка
Сегодня в магазинах можно увидеть большое количество батареек, они различны по некоторым принципам, но схема работы у них одна. У любой батарейки есть положительный полюс (анод–цинк Zn), отрицательный полюс (катод–марганец Mg) и электролит (может быть сухим, жидким). Именно эти составляющие и являются основными элементами батарейки. Электрический ток бежит от анода (+) к катоду (—), но между ними обязательно должна быть нагрузка (лампочка, диод, двигатель или что-то ещё). Если нагрузки не будет (соединить «–» с «+» напрямую), то произойдёт короткое замыкание (К.З.).
Катоды выполняют функцию восстановителя, т.е. принимают электроны от прибывшего анода. Электролит это среда, в которой перемещаются ионы, которые образуются в процессе химической реакции. В процессе работы батарейки постепенно образовываются новые вещества, а электроды постепенно разрушаются — батарейка садится.
Вот и вся работа батарейки, кстати, все процессы, проходящие в гальваническом элементе, необратимы, то есть заряжать батарейки нельзя. Кратко говоря о работе батарейки: анод — нагрузка — катод — электролит.
Электролит изначально изготовляли в жидком виде, но это неудобно, так как при переворачивании батарейки она просто не работала. Из-за этого электролит стали загущать, превращать его в сухой вид.
Принцип работы батарейки
Для того чтобы понять принцип функционирования обычной «пальчиковой» батарейки, необходимо иметь общее представление о её устройстве. Итак, любая батарейка состоит из трёх основных элементов — анода, катода и электролита. При этом последний может иметь фактически любое агрегатное состояние: помещённые в соляной раствор катод и анод, в принципе, так же являются «батарейкой», только в непривычном для рядового обывателя виде.
Интересно! Так называемый «вольтов столб», изобретённый Алессандро Вольта, так же имел все необходимые для производства электротока элементы. Он состоял из уложенных друг на друга цинковых и медных пластин, между которыми в качестве «прослойки» помещалась смоченная в кислоте ткань.
Анод в подобных системах – это главный источник электронов, которые, как мы знаем из школьного курса физики, имеют отрицательный заряд. Отрицательно заряженные частицы притягиваются к положительным, а в качестве «плюса» в данном случае выступает поверхность катода.
Но для возникновения электротока этого мало, ведь электронам нужна ещё и своеобразная «магистраль» — среда, которая поддерживала бы взаимодействие катода и анода. Именно здесь «на сцене» появляется электролит – соль, щёлочь или кислота, способные проводить ток.
Разберём принцип действия на конкретном примере: имеется элемент питания, рассчитанный на 18 вольт. Напряжение между электродами в нём стабильно, пока он не включён в сеть. Как только появляется потребитель (к примеру, обычная лампочка), напряжение начинает постепенно снижаться, от «минусового» электрода к «плюсовому» начнёт течь ток, и в электролите произойдёт химическая реакция, направленная на поддержание разности потенциалов между электродами.
Справка. Чем больше энергии требуется потребителю, тем интенсивнее течёт реакция внутри элемента питания и тем быстрее он выйдет из строя.
Обратная реакция
Все типы батареек и элементов имеют сходный тип химической реакции, происходящей для выработки электроэнергии.
Но в некоторых типах элементов или батарей химические вещества различны, и реакция может быть обратной. Таким образом, элементы могут быть перезаряжены — так же, как литий-ионные аккумуляторы в автомобилях или смартфонах.
Раньше было гораздо дешевле производить неперезаряжаемые элементы, такие как щелочные элементы, поэтому они использовались очень широко.
Но теперь, когда люди осознали, насколько вредно для окружающей среды просто выбрасывать неперезаряжаемые элементы, а поскольку перезаряжаемые элементы становятся дешевле, мы, вероятно, будем использовать неперезаряжаемые элементы все меньше и меньше в будущем.
Типы батареек
- Солевые (угольно-цинковые, марганцево-цинковые) батарейки.
Что это такое солевые батарейки
Солевая батарейка изготавливается из пассивного угля и двуокиси марганца, электролит из хлорида аммония и катод из цинка. В перерывах работы элементы питания могут восстанавливаться, т.е. выравнивать локальные неоднородности в композите электролита, вызванных разрядом. Такой процесс немного продлевает срок службы батарейки.
- Алкалиновые (щёлочные) батарейки
Алкалиновые (щелочные) батарейки что это такое
В отличие от солевых батарей у алкалиновой батарейки химический элемент электролита — щелочной. Щёлочные батарейки (алкалин) имеют продолжительный срок хранения, а в процессе эксплуатации напряжение на электродах меняется гораздо меньше, чем у элементов с солевым раствором.
- Литиевые батарейки — li ion
Литиевые батарейки что это такое
Самые современные. В отличие от щелочных и солевых батареек, в состав катода входит литий (Li – наивысший отрицательный потенциал), в состав анода — различные материалы. Электролит — органический электролит. В связи с такими элементами литиевые батарейки получили большой срок хранения, большую плотность энергии и различную рабочую температуру.
Элементы питания
О. Курапов
Взгляните на свой сотовый телефон, КПК или ноутбук: благодаря стремительному технологическому прогрессу широко доступными стали устройства, которые еще лет десять-пятнадцать назад можно было увидеть лишь в фантастических фильмах. Среди этого расцветшего буйным цветом хайтека совершеннейшим анахронизмом представляется обычная батарейка. Подумать только, принципы, лежащие в основе всех современных элементов питания, были открыты даже не в прошлом веке, а гораздо раньше. И с тех пор они претерпели не столь большие изменения, которые в основном заключались в уменьшении размеров и применении более совершенных материалов.
Казалось бы, в мире гигагерц и нанотехнологий такое «старье» должно отойти на задний план. Но с появлением большого количества современных мобильных устройств (плееров, КПК, фото- и видеокамер, ноутбуков etc.) мы наблюдаем обратную тенденцию – аккумуляторы и батарейки стали не менее важной деталью, чем процессоры. Все зависит именно от емкости источника питания. А без него даже самый навороченный гэджет будет абсолютно бесполезен.
Вообще-то солидный возраст технологии – это даже хорошо. За этот срок ученые и исследователи изучили проблему во всех подробностях. Современные «дураселлы» далеко ушли от батарей Вольты двухвековой давности. И теперь производители тратят очень большие деньги на улучшение параметров своих изделий и уменьшение их размеров. А двигателем этого процесса является постоянное стремление производителей электроники к миниатюризации.
Все последние разработки в этой сфере пытаются удовлетворить потребности современной мобильной техники. Дело в том, что они даже работают по-новому, совсем не так, как радиоприемники или фонарики. Всем этим цифровым камерам, карманным компьютерам и CD-MD-MMC-MP3-плеерам необходимы батарейки, которые выдерживают резкие скачки напряжения, возникающие во время включения экранов, раскручивания дисков и выхода устройств из «спячки».
В отличие от компьютерных компаний, свято чтящих закон Мура, у фирм, выпускающих элементы питания, нет иллюзий по поводу ближайшего (и даже не очень) будущего. Предыдущие десятилетия научили их не ждать чудесного появления новых технологий, которые увеличат емкость батарей вдвое. Напротив, надо кропотливо работать, постепенно улучшая имеющиеся. Достаточно сказать, что за десять лет существования литий-полимерных батарей ресурс этой технологии еще исчерпан не полностью, и лучшие умы отрасли продолжают по проценту, по полпроцента увеличивать их удельную емкость.
Батареи прошли долгий путь развития, но им предстоит еще немало послужить людям. Далее мы расскажем вам об истории создания батареек, а также попытаемся понять, что ждет их впереди. Ну а для начала разберемся, как они работают и что у них внутри.
Батареи – это устройства, накапливающие энергию, которую они потом отдают потребляющему эту самую энергию устройству. Впрочем, под такое определение подпадают также маховики или, скажем, часовые пружины. К сожалению, на данный момент на российском рынке заводные модели сотовых телефонов или КПК не представлены совсем, поэтому оставим эту интересную тему до лучших времен. Опустим также рассказ про свинцовые аккумуляторные батареи – несмотря на то, что они имеют огромную емкость, их мобильность (не путайте с автомобильностью) оставляет желать лучшего.
То, что мы обычно подразумеваем под словом «батарея», можно описать следующими словами: изолированная система, в которой протекают химические процессы, в результате которых вырабатывается электрическая энергия.
Появление переносных компьютеров, а также множества других мобильных «штучек» дало новый толчок к развитию технологий автономного питания. Обычные компьютеры питаются от сети, а потому практически не используют батареи. В качестве исключений можно назвать CMOS-батарейку на материнской плате, аккумуляторы устройств бесперебойного питания (UPS), ну и «пальчики», которые вставляются в разного рода беспроводные мыши, клавиатуры и т. п. То ли дело мобильные устройства: тут даже спорить не о чем, трудно назвать хотя бы одно, в котором бы не стояла батарейка (или аккумулятор).
При всем разнообразии форм и размеров устройств, все они используют практически одинаковые элементы питания. То есть, скажем, и мобильный телефон, и ноутбук оснащаются одними и теми же Li-Ion-аккумуляторами, хотя по форме и емкости их сравнивать трудно.
Принципиальная схема всех батарей, производимых для массового потребителя, практически одинакова. Два электрода – катод и анод – изготавливаются из двух разных металлов (строго говоря, они должны иметь различную степень окисления). Пространство между ними заполнено третьим материалом, называемым электролитом. Широкий выбор компонентов позволяет создавать по единой схеме множество типов батарей, имеющих порой диаметрально противоположные свойства, различную удельную емкость (отношение максимального заряда батареи к ее объему) и номинальное напряжение.
История
Принято считать, что основные принципы работы батарей, использующиеся и по сей день, были открыты в конце XVIII века итальянским физиком и естествоиспытателем Алессандро Вольтой (1745-1827). Именно тогда, работая в университете города Павия, он заинтересовался «животным электричеством», открытым несколькими годами ранее его соотечественником Луиджи Гальвани (в его честь электрохимические элементы питания часто называют гальваническими). Вольта доказал, что именно ток, вырабатываемый при контакте двух различных металлов, вызывает наблюдавшееся сокращение мышц в лягушачьих лапках. Этим он опроверг предположение Гальвани о том, что электричество вырабатывается в самих мышцах. Для того, чтобы доказать свою точку зрения, он наполнил соляным раствором две чаши и соединил их металлическими дугами. Один конец этих дуг был медным, а другой цинковым. Они были установлены так, что в каждой чаше было по одному электроду каждого типа. Эта конструкция и стала первой батареей, вырабатывающей электричество за счет химического взаимодействия двух металлов в растворе. В 1800 г. он усовершенствовал ее, создав свой знаменитый «вольтов столб», первый источник постоянного тока. Он представлял собой 20 пар кружочков, изготовленных из двух различных металлов, проложенных кусочками кожи или ткани, смоченными в соляном растворе. В знак признания заслуг итальянского ученого, его именем была названа единица электрического напряжения – вольт.
Электрохимический элемент
На полученные результаты обратили внимание другие экспериментаторы. Они усовершенствовали вольтов столб, создав новые типы батарей. К примеру, в 1836 г. английский химик Джон Дэниелл поместил медные и цинковые электроды в емкость с серной кислотой. Эта батарея получила название «плоскостной элемент» или «элемент Дэниела». Три года спустя другой англичанин, Уильям Р. Гроув, добавил окислитель для предотвращения накопления водорода около катода, что приводило к снижению напряжения на выходе. Были и другие попытки улучшить первоначальную конструкцию, но ни одно из этих примитивных устройств не используется в наши дни.
Первый значительный прорыв был совершен французом Гастоном Плантэ. В 1859 г. он провел интересный опыт, внешне похожий на то, что проделал Вольта. В его гальваническом элементе в качестве электродов использовались свинцовые пластины, а электролитом являлась разбавленная серная кислота. Плантэ подключил к элементам источник постоянного тока и некоторое время заряжал батарею. После этого прибор стал сам вырабатывать электричество, выдавая почти всю энергию, потраченную на зарядку. Причем подзаряжать его можно было много раз. Именно так и появился тот самый свинцовый аккумулятор, который еще долго будет использоваться во всех производимых автомобилях.
Еще один прибор-долгожитель был разработан и запатентован другим французским изобретателем Жоржем Лекланше в 1866 году. Названный в его честь элемент послужил прообразом современных «сухих» батарей, правда, изначально он такому названию не соответствовал. Дело в том, что в варианте, предложенном Лекланше, электролит был жидким. В производимых же сейчас батарейках он заменен на желеобразный для того, чтобы не допустить вытекания содержимого и порчи оборудования, которое эта батарея питает. В остальном же за это время технология почти не изменилась. Как и полтора века назад, сухие элементы представляют собой цинковый стаканчик (анод), в который вставлен графитовый стержень (катод), а внутреннее пространство заполнено электролитом. По такой технологии выпускают самые дешевые и массовые источники питания, которые вставляют в фонарики, плееры, детские игрушки и т. п.
Впрочем, в своем оригинальном «мокром» виде элементы Лекланше не были ни компактными, ни надежными. Поэтому многочисленные рационализаторы многократно пытались улучшить его потребительские качества, например, помещая в герметичную упаковку, не допускающую утечки электролита.
Типы батарей
Большинство современных аккумуляторных батарей – никель-кадмиевые, никель-металл-гидридные, а также все литиевые – были разработаны уже в 20-ом веке в лабораториях крупных компаний или университетов. Новые химические системы не изобретаются энтузиастами-одиночками, основывающимися на их собственной интуиции. Основные принципы, на которых основано функционирование батарей, уже досконально изучены и описаны точными формулами. Сегодня основные задачи, которые стоят перед разработчиками – это подбор оптимальных компонентов.
Химики различают гальванические элементы двух родов: первого и второго. Разница между ними заключается в том, как производится энергия, которую они вырабатывают.
– это одноразовые батареи, которые производят электроэнергию за счет химических реакций, в результате которых анод, катод и электролит претерпевают необратимые изменения. Это делает перезарядку таких батарей невозможной или очень нерациональной (к примеру, для зарядки некоторых типов батарей придется потратить в десятки раз больше энергии, чем они могут сохранить, а другие виды могут накопить только малую часть своего первоначального заряда). После этого батарею останется только выкинуть в мусорный ящик, откуда, как хотелось бы надеяться, она попадет в переработку (а скорее всего – на свалку).
чаще называют аккумуляторами. Это значит, что они могут заряжаться, если к электродам подключить источник постоянного тока. Химические реакции, протекающие в них, являются обратимыми. Таким образом, батареи второго рода не производят, а лишь сохраняют энергию.
При прочих равных аккумуляторы кажутся лучшим выбором по сравнению с одноразовыми батареями. Используя их, мы не наносим столько вреда окружающей среде, ведь после разрядки их не нужно выбрасывать. Один аккумулятор можно использовать около года, а обычных батареек на этот же срок понадобилось бы штук 100-200, и в каждом элементе содержатся токсичные вещества. Но не все так просто. На деле аккумуляторы имеют несколько серьезных недостатков, которые не позволяют им вытеснить все остальные батареи. В случае срочной необходимости одноразовые батарейки являются лучшим выбором. Они дешевы и всегда готовы к работе. Но для мобильных устройств, используемых регулярно, аккумуляторы продолжают оставаться наиболее выгодным вариантом.
Ни одна батарея не может хранить энергию вечно. Химические вещества внутри реагируют между собой и постепенно разлагаются. В результате снижается заряд батареи. У этой постепенной разрядки есть две основные причины.
Некоторые химические реакции влияют на способность хранить энергию. Через некоторое время батарея потеряет весь свой заряд. Этот промежуток времени, называемый сроком хранения, обычно указывается на ее корпусе. Он зависит от типа и конструкции батарей, но условия хранения также влияют на продолжительность их жизни. Современные литиевые батареи могут храниться более десяти лет, в то же время элементы других типов могут разрядиться за пару недель (к примеру, цинк-воздушные батареи после начала использования). Но даже самые «долгоиграющие» образцы могут прийти в негодность гораздо раньше, если они будут храниться в неблагоприятных условиях. Особенно сильно сказывается влияние высоких температур. Если же их, наоборот, охладить (а некоторые типы даже заморозить), то это часто помогает сохранить их в лучшем виде на время, значительно большее указанного срока годности.
Обратимые химические реакции в аккумуляторах протекают даже тогда, когда они не используются. Этот процесс называется саморазрядкой. Он является обратимым, также как и обычная разрядка. На скорость саморазрядки влияют те же факторы, что и на срок хранения, поэтому она также может сильно отличаться у разных типов батарей: одни теряют до 10% заряда в день, а другие лишь 1%.
Еще один показатель, который важно знать для каждого типа батарей, это удельная емкость. Она определяется как отношение энергии элемента к его массе или объему и выражается в Ватт-часах на единицу массы или объема. Чем выше этот коэффициент, тем больше энергии может храниться в единице веса, и тем более привлекательна она для использования в переносных устройствах. В этой таблице приведены отношения для различных типов аккумуляторов, выраженные в Вт-ч/кг.
| Тип | Вольтаж | Уд. емкость |
|---|---|---|
| Ni-Cad | 1,2 | 40 – 60 |
| NiMH | 1,2 | 60 – 80 |
| Li-Ion | 3,6 | 90 – 110 |
| Li-Polymer | 3,6 | 130 – 150 |
Химические системы
Одним из важнейших факторов при разработке батарей (а также любого устройства, питающегося от них) является достижение максимальной удельной емкости для элемента заданного (минимального) размера и веса. Химические реакции, протекающие внутри элемента, определяют и его емкость, и физические размеры. В принципе вся история разработки батарей сводится к нахождению новых химических систем и упаковке их в корпуса как можно меньших размеров.
Сегодня производится множество разных типов элементов питания, некоторые из которых были разработаны еще в 19-ом веке, а другие едва отметили десятилетие. Такое разнообразие объясняется тем, что каждая технология имеет свои сильные стороны. Мы расскажем о самых распространенных из тех, что используются в мобильных устройствах.
Сухие батареи
Первыми серийно выпускаемыми элементами питания стали именно сухие. Наследники изобретения Лекланше, они являются самыми распространенными в мире. Одна лишь компания Energizer продает более 6 миллиардов таких батарей ежегодно. В общем, «говорим – батарейка, подразумеваем – сухой элемент». И это несмотря на то, что они имеют самую низкую удельную емкость из всех «массовых» типов. Объясняется такая популярность, во-первых, их дешевизной, а во-вторых, тем, что этим именем называют сразу три разных химических системы: хлорно-цинковые, щелочные и марганцево-цинковые батареи (элементы Лекланше). Их имена дают представление о химических системах, на базе которых они созданы.
В сухих элементах по оси батарейки расположен угольный стержень токосъемника катода. Сам катод – это целая система, в которую входят диоксид марганца, уголь электрода и электролит. Цинковый «стаканчик» служит анодом и образует металлический корпус элемента. Электролит, в свою очередь, также представляет собой смесь, в которую входят нашатырь, диоксид марганца и хлорид цинка.
Марганцево-цинковые и хлорно-цинковые элементы отличаются, по сути, электролитом. Первые содержат в себе смесь нашатыря и хлорида цинка, разбавленную водой. Во вторых электролит почти на 100% представляет собой хлорид цинка. Различие в номинальном напряжении у них минимально: 1,55 В и 1,6 В соответственно.
Несмотря на то, что хлорно-цинковые имеют большую емкость по сравнению с элементами Лекланше, это преимущество пропадает при малой нагрузке. Поэтому на них часто пишут «heavy-duty», то есть элементы с повышенной мощностью. Как бы то ни было, эффективность всех сухих элементов сильно падает при увеличении нагрузки. Именно поэтому в современные фотоаппараты их ставить не стоит, они просто для этого не предназначены.
Сколько бы не бегали розовые зайчики в рекламе, щелочные батарейки – это все те же угольно-цинковые ископаемые родом из 19-го века. Единственное отличие заключается в специально подобранной смеси электролита, позволяющей добиться увеличения емкости и срока хранения таких батареек. В чем секрет? Эта смесь является несколько более щелочной, чем у двух других типов.
Если химический состав у щелочных батареек мало отличается от оного у элемента Лекланше, то в конструкции различия существенны. Можно сказать, что щелочная батарея – это сухой элемент, вывернутый наизнанку. Внешний корпус у них не является анодом, это просто защитная оболочка. Анодом здесь является желеобразная смесь цинкового порошка вперемешку с электролитом (который в свою очередь является водным раствором гидроксида калия). Катод, смесь угля и диоксида марганца, окружает анод и электролит. Он отделяется слоем нетканого материала, например полиэстера.
В зависимости от области применения щелочные батарейки могут прослужить в 4-5 раз дольше, чем обычные угольно-цинковые. Особенно заметна эта разница при таком режиме использования, когда короткие периоды высокой нагрузки перемежаются длительными периодами бездействия.
Важно помнить, что щелочные батарейки не являются перезаряжаемыми, потому что химические процессы, на которых они основаны, не являются обратимыми. Если ее поставить в зарядное устройство, то она будет вести себя не как аккумулятор, а скорее как резистор – начнет нагреваться. Если ее оттуда вовремя не вынуть, то она нагреется достаточно сильно, чтобы взорваться.
Никель-кадмиевые аккумуляторы
Название подсказывает нам, что батареи этого типа имеют никелевый анод и кадмиевый катод. Никель-кадмиевые аккумуляторы (обозначаются Ni-Cad) пользуются заслуженной популярностью у потребителей во всем мире. Не в последнюю очередь это объясняется тем, что они выдерживают большое количество циклов зарядки-разрядки – 500 и даже 1000 – без существенного ухудшения характеристик. Кроме того они, относительно легкие и энергоемкие (хотя их удельная емкость приблизительно в два раза меньше, чем у щелочных батареек). С другой стороны, они содержат токсичный кадмий, так что с ними надо быть поаккуратнее, как во время использования, так и после, при утилизации.
Напряжение на выходе у большинства батарей падает по мере разрядки, потому что в результате химических реакций увеличивается их внутреннее сопротивление. Никель-кадмиевые батареи характеризуются очень низким внутренним сопротивлением, а потому могут подать на выход достаточно сильный ток, который к тому же практически не изменяется по мере разрядки. Следовательно, напряжение на выходе также остается почти неизменным до тех пор, пока заряд почти совсем не иссякнет. Тогда напряжение на выходе резко падает практически до нуля.
Постоянный уровень выходного напряжения является преимуществом при проектировании электрических схем, но это же делает определение текущего уровня заряда практически невозможным. Из-за такой особенности остаток энергии вычисляется на основе времени работы и известной емкости конкретного типа батарей, а потому является величиной приблизительной.
Гораздо более серьезным недостатком является «эффект памяти». Если такую батарею разрядить не полностью, а потом поставить заряжаться, то их емкость может уменьшиться. Дело в том, что при такой «неправильной» зарядке на аноде образуются кристаллы кадмия. Они и играют роль химической «памяти» батарейки, запоминая этот промежуточный уровень. Когда во время следующей разрядки заряд батареи упадет до этого уровня, выходное напряжение понизится так же, как если бы батарейка была полностью разряжена. «Злопамятные» кристаллы будут продолжать формироваться на аноде, усиливая влияние этого неприятного эффекта. Чтобы избавиться от него, нужно продолжить разрядку после достижения этого промежуточного уровня. Только таким образом можно «стереть» память и восстановить полную емкость батареи.
Этот прием обычно называют глубокой разрядкой. Но глубокая не значит полная, «до нуля». Это лишь укоротит срок службы элемента. Если в процессе использования напряжение на выходе упадет ниже отметки 1 В (при номинальном напряжении 1,2 В), то это уже может привести к порче батарейки. Сложная техника, например КПК или ноутбуки, настроены таким образом, чтобы они отключались прежде чем заряд аккумулятора упадет ниже предельного уровня. Для глубокой разрядки батарей нужно использовать специальные приборы, которые выпускают многие известные фирмы.
Некоторые компании-производители заявляют, что новые никель-кадмиевые аккумуляторы не подвержены влиянию эффекта памяти. Впрочем, на практике это не было доказано.
Что бы там не обещали производители, для достижения максимальной отдачи батареи следует каждый раз полностью заряжать, а потом дожидаться нормальной разрядки, чтобы они не испортились и прослужили весь срок.
Предотвращение электролиза
В результате электролиза внутри никель-кадмиевых аккумуляторов могут накапливаться потенциально взрывоопасные газы: водород и кислород. Чтобы не допустить этого, батареи помещаются в герметичную оболочку. В ней имеются специальные микроклапаны, предназначенные для автоматического стравливания накопившихся газов. Они настолько малы, что заметить их очень сложно. Важно, чтобы эти клапаны не оказались закрыты, поэтому батареи не стоит заворачивать, склеивать или обматывать скотчем.
Никель-металл-гидридные аккумуляторы
С точки зрения химии идеальным материалом для катода был бы водород. Но в обычных условиях использовать его для этого невозможно. При комнатной температуре и атмосферном давлении он является газом, и его проще использовать для наполнения аэростатов, чем в качестве материала для батарей.
Впрочем, еще в конце 60-х годов XX века ученые открыли ряд сплавов, способных связывать атомарный водород в объеме, в 1000 раз превышающем их собственный. Они получили название гидриды, а химически они обычно представляют соединения таких металлов, как цинк, литий и никель. При грамотном использовании с помощью гидридов можно хранить достаточно водорода, чтобы использовать его в обратимых реакциях внутри аккумуляторов.
Наибольшее распространение получили никель-металл-гидридные (NiMH) батареи, имеющие гидридный катод и никелевый анод.
Использование гидридов имеет несколько преимуществ. Наиболее очевидным является то, что в производстве не используется токсичный кадмий. Отсутствие этого материала также означает, что такие батареи должны быть свободны от эффекта памяти. Кроме того, благодаря использованию водорода в качестве катода, удалось добиться 50-процентного увеличения удельной емкости (по сравнению с никель-кадмиевыми батареями). На практике это значит, что с никель-металл-гидридными аккумуляторами плеер или другое подобное устройство будет работать на 50% дольше.
Но применение водорода приносит не только положительные, но и отрицательные результаты. Главным недостатком является то, что эти батареи существенно сильнее подвержены саморазрядке. Некоторые из них теряют до 5% заряда за день, хотя в последних моделях этот показателей удалось снизить.
График разрядки никель-металл-гидридных аккумуляторов под нагрузкой немного отличается от никель-кадмиевых. По номинальному напряжению они не различаются (все те же 1,2 В). Но если батарея была полностью заряжена, то в течение некоторого времени напряжение на выходе составляет 1,4 В. После этого короткого промежутка оно падает до уровня 1,2 В, и дальше NiMH-батареи ведут себя так же, как и NiCad.
Оба типа вообще имеют достаточно похожие свойства. NiMh-батареи также могут вырабатывать ток большой силы, выдерживают много циклов зарядки/разрядки (обычно около 500). Но все же это две разные технологии.
Если во время разрядки батареи двух этих типов ведут себя почти одинаково, то при зарядке сходства не наблюдается. Говоря конкретно, никель-кадмиевые батареи при зарядке практически не изменяют свою температуру. Никель-металл-гидридные вырабатывают тепло, причем при достижении полного заряда они могут нагреться весьма значительно. Из-за этого для разных батарей нужны разные зарядные устройства. И хотя на рынке присутствуют универсальные приборы, обычно единовременно в них можно заряжать аккумуляторы только одного типа.
Литий-ионные аккумуляторы
Литий является самым химически активным металлом и используется именно в компактных системах, обеспечивающих энергией современную мобильную технику. Литиевые катоды используются практически во всех батареях с большой емкостью. Но благодаря активности этого металла батареи получаются не только очень емкими, они также имеют самое высокое номинальное напряжение. В зависимости от анода литий-содержащие элементы имеют выходное напряжение от 1,5 В до 3,6 В!
Основной проблемой при использовании лития опять-таки является его высокая активность. Он даже может вспыхнуть – что говорить, не самая приятная особенность, когда речь идет о батареях. Из-за этих проблем элементы на базе металлического лития, которые начали появляться еще в 70х-80х годах XX века, «прославились» своей низкой надежностью.
Чтобы избавиться от этих трудностей, производители батарей постарались использовать литий в виде ионов. Таким образом им удалось получить все полезные электрохимические качества, не связываясь с капризной металлической формой.
В литий-ионных элементах ионы лития связаны молекулами других материалов. Типичный Li-Ion-аккумулятор имеет угольный анод и катод из литийкобальтдиоксида. Электролит в своей основе имеет раствор солей лития.
Литиевые батареи имеют большую плотность, нежели никель-металл-гидридные. Скажем, в ноутбуках такие аккумуляторы могут работать в полтора раза дольше никель-металл-гидридных. Кроме того, литий-ионные элементы избавлены от эффектов памяти, которыми страдали ранние никель-кадмиевые батареи.
С другой стороны, внутреннее сопротивление у современных литиевых элементов выше, чем у никель-кадмиевых. Соответственно, они не могут обеспечить такие сильные токи. Если никель-кадмиевые элементы способны расплавить монету, то литиевые на это не способны. Но все равно мощности таких батареек вполне хватит для работы ноутбука, если это не связано со скачкообразными нагрузками (это значит, что некоторые устройства, например, винчестер или CD-ROM, не должны вызывать высоких скачков на предельных режимах – например, при начальной раскрутке или выходе из спящего режима). Более того, даже несмотря на то, что литий-ионные батарейки выдержат не одну сотню подзарядок, они живут меньше, чем те, в которых используется никель.
Из-за того, что в литий-ионных элементах используется жидкий электролит (пусть даже отделенный слоем ткани), по форме они почти всегда являются цилиндром. Хотя такая форма ничуть не хуже форм других элементов, с появлением полимеризованных электролитов литий-ионные батареи становятся компактнее.
Литий-полимерные аккумуляторы
Наиболее продвинутой технологией, используемой сегодня при создании аккумуляторов, является литий-полимерная. Уже сейчас среди производителей как батарей, так и компьютерных устройств наметилась тенденция постепенного перехода к этому типу элементов. Главным преимуществом литий-полимерных батарей является отсутствие жидкого электролита. Нет, это не значит, что ученые нашли способ обходиться совсем без электролита. Анод отделен от катода полимерной перегородкой, композитным материалом, таким, как полиакрилонитрит, который содержит литиевую соль.
Благодаря отсутствию жидких компонентов литий-полимерные элементы могут иметь практически любую форму, в отличие от цилиндрических батарей других типов. Обычными формами упаковки для них являются плоские пластины или бруски. В таком виде они лучше заполняют пространство батарейного отсека. В результате при одинаковой удельной плотности, литий-полимерные батареи оптимальной формы могут хранить на 22% больше энергии, чем аналогичные литий-ионные. Это достигается за счет заполнения «мертвых» объемов в углах отсека, которые остались бы неиспользованными в случае применения цилиндрической батареи.
Кроме этих очевидных преимуществ, литий-полимерные элементы являются экологически безопасными и более легкими за счет отсутствия внешнего металлического корпуса.
Литий-железодисульфидные батареи
В отличие от других литий-содержащих батарей, которые имеют выходное напряжение более 3 В, у литий-железодисульфидных оно в два раза меньше. Кроме того, их нельзя перезаряжать. Эта технология представляет собой некий компромисс, на который разработчики пошли, чтобы обеспечить совместимость литиевых источников питания с техникой, разработанной для использования щелочных батареек.
Химический состав батарей был специальным образом изменен. В них литиевый анод отделен от железодисульфидного катода прослойкой электролита. Этот сэндвич упаковывается в герметичный корпус с микроклапанами для вентиляции, как и никель-кадмиевые батареи.
Этот тип элементов был задуман как конкурент щелочным батарейкам. По сравнению с ними литий-железодисульфидные весят на треть меньше, имеют большую емкость, а, кроме того, еще и хранятся дольше. Даже после десяти лет хранения они сохраняют почти весь свой заряд.
Превосходство над конкурентами проявляется наилучшим образом при большой нагрузке. В случае высоких токов нагрузки литий-железодисульфидные элементы могут работать в 2,5 раза дольше, чем алкалиновые батареи того же размера. Если же на выходе не требуется высокая сила тока, то разница заметна гораздо меньше. К примеру, один из производителей элементов питания заявил следующие характеристики двух типов своих батарей размера AA: при нагрузке 20 мА щелочная батарейка проработает 122 часа против 135 часов у литий-железодисульфидной. Если же нагрузку увеличить до 1А, то продолжительность работы составит 0,8 и 2,1 часа соответственно. Как говорится, результат налицо.
Такие мощные батареи нет смысла ставить в устройства, потребляющие относительно немного энергии в течение длительного времени. Они были специально созданы для использования в фотоаппаратах, мощных фонарях, а в будильник или радиоприемник лучше поставить щелочные батарейки.
Зарядные устройства
Современные устройства для подзарядки – это сложные электронные приборы, оснащенные различными системами защиты – как вашей, так и ваших батареек. В большинстве случаев каждому типа элементов нужно своё собственное зарядное устройство. При неправильном использовании можно испортить не только батарейки, но и сам зарядник.
Существует два режима работы зарядных устройств – с постоянным напряжением и с постоянным током.
Устройства, работающие только с постоянным напряжением, являются самыми простыми. Они всегда подают одно и то же напряжение, но сила тока зависит от уровня заряда батарейки и других факторов. По мере накопления энергии напряжение батареи увеличивается, а значит, уменьшается разница потенциалов зарядного устройства и батареи. В результате сила тока в цепи уменьшается.
Устроены они несложно, все, что нужно – трансформатор (для уменьшения напряжения в сети до нужного уровня) и выпрямитель (для преобразования переменного тока в постоянный). Такими устройствами комплектуются некоторые литий-ионные батареи, правда, в них обычно добавляют системы защиты от перезарядки.
Второй вид зарядных устройств обеспечивает постоянную силу тока и изменяет напряжение для обеспечения требуемой величины тока. Зарядка прекращается, когда напряжение батарейки достигает уровня полного заряда. Обычно такие устройства применяются для никель-кадмиевых и никель-металл-гидридных элементов. Чтобы не испортить батарейку, нужно остановить зарядку после достижения нужного уровня. В зависимости от вида батареи и «навороченности» зарядного устройства для определения необходимого времени подзарядки используются различные технологии.
В самых простых случаях измеряется напряжение, вырабатываемое батарейкой. Система следит за напряжением и разрывает цепь в тот момент, когда оно достигает порогового уровня. Но такой способ подходит далеко не для всех элементов. К примеру, этого никогда не встретишь в зарядных устройствах для никель-кадмиевых аккумуляторов, у которых кривая разряда является практически прямой большую часть времени. Это делает определение порогового напряжения невозможным.
Более сложные зарядные устройства выбирают режим работы, основываясь на измерении температуры элемента. Когда батарея начинает нагреваться, они уменьшают силу тока. Обычно в такие элементы питания встраиваются термометры, которые следят за температурой элемента и передают зарядному устройству соответствующий сигнал.
Наиболее продвинутые устройства используют оба метода сразу. Они начинают с большого тока, а потом, обрабатывая данные с датчиков напряжения и температуры, могут переключиться на малый. Если батарея уже заряжена, то они переходят в режим поддержания заряда. В этом случае батарейка подзаряжается лишь слегка, чтобы компенсировать процесс саморазряда. Ток заряда при этом составляет лишь одну двадцатую, одну тридцатую номинального тока разряда батарейки. Но для этого батарея должна поддерживать режим зарядки малым током (к примеру, никель-кадмиевые так заряжать нельзя). Большинство зарядных устройств для ноутбуков и сотовых телефонов специально разработаны таким образом, что могут постоянно быть подключены к элементам.
Хранение
Если вы хотите, чтобы ваши батареи служили как можно дольше, то о них надо заботиться. С элементами первого рода, то есть с одноразовыми батареями, попроще, их важно лишь правильно хранить, а после использования их все равно выбрасывают. Аккумуляторы, элементы второго рода, требуют больше внимания, потому что их нужно регулярно заряжать.
Все аккумуляторы при перегреве портятся. Причем губительной может стать даже зарядка, если ее во время не остановить. Ничего страшного нет в том, что ваш аккумулятор слегка нагревается, когда он подключен к зарядному устройству. Но при излишней зарядке температура поднимается значительно, батарея становится горячей, а это верный знак того, что больше ее зарядить не удастся.
Аккумулятор также может прийти в негодность, если его полностью разрядить. Это может быть вызвано коротким замыканием. Кстати, интересный факт: некоторые батареи после разрядки ниже рекомендуемого уровня могут поменять полярность! В общем, если ваш ноутбук предупреждает вас о том, что его батареи почти полностью разряжены, не пытайтесь продолжить работу – дороже выйдет.
Большинство перезаряжаемых батарей лучше хранятся в разряженном состоянии. Особенно это относится к никель-кадмиевым элементам. Поэтому те батареи, которые долго лежат на складе, обычно продаются незаряженными.
Устройства
Большая часть устройств предполагает использование батарей одного из стандартных размеров, например, AA, AAA и тому подобное. Поэтому у покупателей есть выбор, элементы какого типа предпочесть.
Надпись»Heavy-duty» (высокая нагрузка), которую можно увидеть на некоторых угольно-цинковых батарейках – не просто рекламный ход. Это означает, что они предназначены для использования в устройствах, нуждающихся в токе большой силы. Пример таких устройств – фонари, электромоторы и все приборы, в которых они применяются, например детские игрушки. Там эти батареи прослужат гораздо дольше, чем обычные. Если же прибор потребляет мало электроэнергии, то преимущество почти будет почти незаметно.
Разные литий-содержащие батарейки сильно отличаются друг от друга в том, что касается области применения. Литий-железодисульфидные являются рекордсменами при работе с большими нагрузками. Другие типы, например литиевые часовые батарейки, применяются там, где нагрузки, наоборот, не велики. Литий-ионные и литий-полимерные находятся где-то посередине, а потому являются наиболее универсальными.
Там, где могут быть использованы и аккумуляторы, и одноразовые батарейки, предпочтительнее обычно оказываются первые. Но в некоторых случаях их преимущества бывают не востребованы. Возьмем, к примеру, пульт дистанционного управления, который потребляет очень мало энергии, но используется постоянно и на протяжении длительного времени. Обычные батарейки могут прослужить в нем несколько лет, а аккумуляторы вообще столько не живут, к тому же на таких длительных промежутках времени дает о себе знать гораздо более высокая скорость саморазрядки этих элементов. На другом полюсе находятся устройства, которые используются редко, но должны быть всегда готовы к работе в случае необходимости. В них тоже лучше поставить что-нибудь одноразовое, но «долгоиграющее». В общем, принцип понятен – нет самой лучшей батареи или аккумулятора, для каждого конкретного применения что-то будет хорошо, а что-то плохо.
Напоследок повторим несколько важных правил:
- Если какой-то металлический предмет закоротит контакты батареи, то она начнет нагреваться. Это может вызвать порчу вашего имущества и даже пожар.
- Большинство аккумуляторов вырабатывает водород в процессе электролиза, вызванного перезарядкой. Герметизация корпусов современных батарей значительно уменьшает риск утечек и возгорания газа, но полной гарантии никто дать не может, потому что встроенные клапаны периодически выпускают излишки скопившегося водорода.
- Гораздо большую опасность несет газ, который не может покинуть корпус. Если по какой-то причине автоматические клапаны оказались заблокированы, при повышении температуры давлении внутри может вырасти настолько, что батарея взорвется. Поэтому корпус аккумуляторов никогда не должен заклеиваться, запаиваться в пластик и тому подобное.
- Почти все батареи содержат опасные химические соединения: токсичные, ядовитые, легковоспламеняющиеся – это зависит от технологии. Поэтому важно, чтобы они были правильно утилизированы после использования. Понятное дело, что все равно все это окажется на ближайшей свалке, но уж лучше пусть они лежат где-нибудь далеко, чем валяются на улице.
Статья опубликована на сайте HPC.RU.
Перепечатывается с разрешения редакции.
Как работает аккумулятор — Любопытно
Представьте себе мир без батарей. Все портативные устройства, от которых мы так зависим, были бы настолько ограничены! Мы сможем доставить наши ноутбуки и телефоны настолько далеко, насколько это досягаемо для их кабелей, что сделает это новое работающее приложение, которое вы только что загрузили на свой телефон, практически бесполезным.
К счастью, батарейки у нас есть. Еще в 150 г. до н.э. в Месопотамии парфянская культура использовала устройство, известное как багдадская батарея, сделанное из медных и железных электродов с уксусом или лимонной кислотой.Археологи считают, что на самом деле это не батареи, а в основном они использовались для религиозных церемоний.
Изобретение батареи в том виде, в котором мы ее знаем, приписывают итальянскому ученому Алессандро Вольта, который собрал первую батарею, чтобы доказать свою точку зрения другому итальянскому ученому Луиджи Гальвани. В 1780 году Гальвани показал, что лапки лягушек, подвешенных на железных или латунных крючках, подергиваются при прикосновении к зонду из другого металла. Он считал, что это было вызвано электричеством из тканей лягушек, и называл это «животным электричеством».
Луиджи Гальвани обнаружил, что лапы лягушек, подвешенных на латунных крючках, дергались, когда их ткнули зондом из другого металла. Он думал, что эта реакция была вызвана «животным электричеством» внутри лягушки. Источник изображения: Луиджи Гальвани / Wikimedia Commons.Вольта, первоначально впечатленный открытиями Гальвани, пришел к выводу, что электрический ток исходит от двух разных типов металла (крючки, на которых висели лягушки, и другой металл зонда) и просто передается через них, а не через них. из тканей лягушек.Он экспериментировал со стопками слоев серебра и цинка, перемежаемых слоями ткани или бумаги, пропитанной соленой водой, и обнаружил, что электрический ток действительно протекает через провод, приложенный к обоим концам стопки.
Батарея Алессандро Вольта: куча цинковых и серебряных листов, перемеженных тканью или бумагой, пропитанной соленой водой. Представьте, что вы используете это для питания вашего телефона. Источник изображения: Луиджи Кьеза / Wikimedia Commons.Volta также обнаружил, что, используя различные металлы в свае, можно увеличить количество напряжения.Он описал свои открытия в письме Джозефу Бэнксу, тогдашнему президенту Лондонского королевского общества, в 1800 году. Это было довольно большое дело (Наполеон был весьма впечатлен!), И его изобретение принесло ему устойчивое признание в честь «вольта». ‘(мера электрического потенциала), названная в его честь.
Я сам, шутя в сторону, поражен тем, как мои старые и новые открытия … чистого и простого электричества, вызванного контактом металлов, могли вызвать такое волнение.Алессандро Вольта
Так что же именно происходило с этими слоями цинка и серебра и с дрожащими лягушачьими лапами?
Химия батареи
Батарея — это устройство, которое накапливает химическую энергию и преобразует ее в электричество.Это известно как электрохимия, а система, лежащая в основе батареи, называется электрохимическим элементом. Батарея может состоять из одного или нескольких (как в оригинальной кучке Вольты) электрохимических ячеек. Каждая электрохимическая ячейка состоит из двух электродов, разделенных электролитом.
Итак, откуда электрохимический элемент получает электричество? Чтобы ответить на этот вопрос, нам нужно знать, что такое электричество. Проще говоря, электричество — это тип энергии, производимый потоком электронов.В электрохимической ячейке электроны образуются в результате химической реакции, которая происходит на одном электроде (подробнее об электродах ниже!), А затем они перетекают на другой электрод, где расходуются. Чтобы понять это должным образом, нам нужно внимательнее изучить компоненты клетки и то, как они устроены вместе.
Электроды
Чтобы создать поток электронов, вам нужно где-то, чтобы электроны текли с из , и где-то электроны текли с по .Это электроды ячейки. Электроны текут от одного электрода, называемого анодом (или отрицательным электродом), к другому электроду, называемому катодом (положительный электрод). Обычно это разные типы металлов или другие химические соединения.
В котле Вольта анодом служил цинк, от которого электроны текли по проволоке (при соединении) с серебром, которое было катодом батареи. Он сложил много этих ячеек вместе, чтобы получилась общая куча, и поднял напряжение.
Но откуда анод вообще берет все эти электроны? И почему они так счастливы, что их отправили в веселый путь к катоду? Все сводится к химии, происходящей внутри клетки.
Нам нужно понять пару химических реакций. На аноде электрод вступает в реакцию с электролитом, в результате чего образуются электроны. Эти электроны накапливаются на аноде. Между тем, на катоде одновременно происходит другая химическая реакция, которая позволяет этому электроду принимать электроны.
Технический химический термин, обозначающий реакцию, которая включает обмен электронами, — это реакция восстановления-окисления, обычно называемая окислительно-восстановительной реакцией. Вся реакция может быть разделена на две половинные реакции, и в случае электрохимической ячейки одна полуреакция происходит на аноде, а другая — на катоде. Уменьшение — это усиление электронов, и это то, что происходит на катоде; мы говорим, что катод восстанавливается во время реакции. Окисление — это потеря электронов, поэтому мы говорим, что анод окисляется.
Каждая из этих реакций имеет определенный стандартный потенциал. Думайте об этой характеристике как о способности / эффективности реакции либо производить, либо поглощать электроны — ее силе в электронном перетягивании каната.
- Стандартные потенциалы для полуреакций
Ниже приведен список половинных реакций, которые включают высвобождение электронов из чистого элемента или химического соединения. Рядом с реакцией указано число (E 0 ), которое сравнивает силу электрохимического потенциала реакции с силой готовности водорода расстаться со своим электроном (если вы посмотрите вниз по списку, вы увидите, что водородная полуреакция имеет нулевое значение E 0 ).E 0 измеряется в вольтах.
Причина, по которой этот список настолько интересен, заключается в том, что если вы выберете две реакции из списка и объедините их в электрохимическую ячейку, значения E 0 скажут вам, в каком направлении будет протекать общая реакция: реакция с более отрицательной реакцией. Значение E 0 отдает свои электроны другой реакции, и это определяет анод и катод вашей ячейки. Разница между двумя значениями E 0 говорит вам об электрохимическом потенциале вашего элемента, который в основном представляет собой напряжение элемента.
Итак, если вы возьмете литий и фторид и сумеете объединить их, чтобы сделать элемент батареи, у вас будет самое высокое напряжение, теоретически достижимое для электрохимического элемента. Этот список также объясняет, почему в котле Вольта цинк был анодом, а серебро — катодом: полуреакция цинка имеет более низкое (более отрицательное) значение E 0 (-0,7618), чем полуреакция серебра (0,7996). .
Источник: UC Davis ChemWiki
Любые два проводящих материала, которые вступают в реакцию с разными стандартными потенциалами, могут образовывать электрохимическую ячейку, потому что более сильный из них сможет забирать электроны у более слабого.Но идеальным выбором для анода был бы материал, который вызывает реакцию со значительно более низким (более отрицательным) стандартным потенциалом, чем материал, который вы выбираете для своего катода. В итоге мы получаем электроны, притягивающиеся к катоду от анода (и анод не очень сильно пытается бороться), и, когда у нас есть легкий путь, чтобы добраться туда — проводящий провод, мы можем использовать их энергию для обеспечения электрического питание нашего фонарика, телефона или чего-то еще.
Разница в стандартном потенциале между электродами как бы равна силе, с которой электроны перемещаются между двумя электродами.Это известно как общий электрохимический потенциал ячейки, и он определяет напряжение ячейки. Чем больше разница, тем больше электрохимический потенциал и выше напряжение.
Чтобы увеличить напряжение аккумулятора, у нас есть два варианта. Мы могли бы выбрать для наших электродов другие материалы, которые придадут ячейке больший электрохимический потенциал. Или мы можем сложить несколько ячеек вместе. Когда элементы объединяются определенным образом (последовательно), это оказывает аддитивное влияние на напряжение батареи.По сути, силу, с которой электроны движутся через батарею, можно рассматривать как общую силу, когда она движется от анода первого элемента на всем пути, сколько бы ячеек ни содержала батарея, к катоду последней ячейки.
Когда элементы объединяются другим способом (параллельно), это увеличивает возможный ток батареи, который можно рассматривать как общее количество электронов, протекающих через элементы, но не ее напряжение.
Электролит
Но электроды — это всего лишь часть батареи.Помните обрывки бумаги Вольты, пропитанные соленой водой? Соленая вода была электролитом, еще одной важной частью картины. Электролит может быть жидкостью, гелем или твердым веществом, но он должен обеспечивать движение заряженных ионов.
Электронов имеют отрицательный заряд, и поскольку мы посылаем поток отрицательных электронов по нашей цепи, нам нужен способ уравновесить это движение заряда. Электролит обеспечивает среду, через которую могут протекать положительные ионы, уравновешивающие заряд.
Поскольку химическая реакция на аноде производит электроны, для поддержания баланса нейтрального заряда на электроде также производится соответствующее количество положительно заряженных ионов. Они не проходят по внешнему проводу (только для электронов!), А попадают в электролит.
В то же время катод должен также уравновешивать отрицательный заряд электронов, которые он принимает, поэтому реакция, которая здесь происходит, должна втягивать положительно заряженные ионы из электролита (альтернативно, он также может высвобождать отрицательно заряженные ионы из электрода в электролит. электролит).
Итак, в то время как внешний провод обеспечивает путь для потока отрицательно заряженных электронов, электролит обеспечивает путь для переноса положительно заряженных ионов, чтобы уравновесить отрицательный поток. Этот поток положительно заряженных ионов так же важен, как и электроны, обеспечивающие электрический ток во внешней цепи, которую мы используем для питания наших устройств. Роль балансировки заряда, которую они выполняют, необходима для поддержания протекания всей реакции.
Итак, если бы все ионы, высвобожденные в электролит, могли полностью свободно перемещаться через электролит, они в конечном итоге покрыли бы поверхности электродов и забили бы всю систему.Таким образом, в клетке обычно есть какой-то барьер, чтобы этого не произошло.
При использовании аккумулятора возникает ситуация, когда происходит непрерывный поток электронов (через внешнюю цепь) и положительно заряженных ионов (через электролит). Если этот непрерывный поток остановлен — если цепь разомкнута, например, когда ваш фонарик выключен — поток электронов остановлен. Заряды будут накапливаться, и химические реакции, приводящие в движение аккумулятор, прекратятся.
По мере использования батареи и протекания реакций на обоих электродах возникают новые химические продукты.Эти продукты реакции могут создавать своего рода сопротивление, которое может помешать продолжению реакции с такой же эффективностью. Когда это сопротивление становится слишком большим, реакция замедляется. Электронное перетягивание каната между катодом и анодом также теряет свою силу, и электроны перестают течь. Аккумулятор медленно разряжается.
Зарядка аккумулятора
Некоторые распространенные батареи предназначены только для одноразового использования (так называемые первичные или одноразовые батареи).Электроны перемещаются от анода к катоду в одну сторону. Либо их электроды истощаются по мере того, как они выделяют свои положительные или отрицательные ионы в электролит, либо накопление продуктов реакции на электродах препятствует продолжению реакции, и это делается и вытирается пыль. Батарея оказывается в мусорном ведре (или, надеюсь, на переработку, но это уже другая тема Nova).
Но. Изящная вещь в этом потоке ионов и электронов, который имеет место в некоторых типах батарей с соответствующими материалами электродов, заключается в том, что он также может двигаться в обратном направлении, возвращая нашу батарею в исходную точку и давая ей совершенно новую жизнь. .Подобно тому, как батареи изменили способ использования различных электрических устройств, аккумуляторные батареи еще больше изменили полезность этих устройств и их продолжительность жизни.
Когда мы подключаем почти разряженную батарею к внешнему источнику электричества и отправляем энергию обратно в батарею, происходит обратная химическая реакция, которая произошла во время разряда. Это отправляет положительные ионы, выпущенные из анода, в электролит, обратно к аноду, а электроны, которые катод принимает, также обратно к аноду.Возврат как положительных ионов, так и электронов обратно в анод подготавливает систему, так что она снова готова к работе: ваша батарея заряжена.
Однако процесс не идеален. Замена отрицательных и положительных ионов электролита обратно на соответствующий электрод при перезарядке аккумулятора не такая аккуратная и не такая хорошо структурированная, как электрод вначале. Каждый цикл зарядки еще больше ухудшает состояние электродов, а это означает, что батарея со временем теряет производительность, поэтому даже аккумуляторные батареи не работают вечно.
В течение нескольких циклов зарядки и разрядки форма кристаллов аккумулятора становится менее упорядоченной. Это усугубляется, когда аккумулятор разряжается / заряжается с высокой скоростью — например, если вы едете на электромобиле с большой скоростью, а не с постоянной скоростью. Высокоскоростное переключение приводит к тому, что кристаллическая структура становится более неупорядоченной, что приводит к менее эффективной батарее.
Эффект памяти и саморазряд
Почти, но не полностью обратимые реакции разряда и перезарядки также способствуют так называемому «эффекту памяти».Когда вы перезаряжаете некоторые типы аккумуляторных батарей, не разрядив их сначала, они «запоминают», где находились в предыдущих циклах разрядки, и не перезаряжаются должным образом.
В некоторых элементах это вызвано тем, как металл и электролит реагируют с образованием соли (и тем, как эта соль затем снова растворяется и металл заменяется на электродах при перезарядке). Мы хотим, чтобы наши клетки имели красивые, однородные, маленькие кристаллы соли, покрывающие идеальную металлическую поверхность, но это не то, что мы получаем в реальном мире! Некоторые кристаллы образуются очень сложно, а некоторые металлы откладываются во время перезарядки, поэтому некоторые типы батарей имеют больший эффект памяти, чем другие.Дефекты в основном зависят от первоначального состояния заряда батареи, температуры, напряжения заряда и тока зарядки. Со временем недостатки в одном цикле зарядки могут вызвать то же самое в следующем цикле зарядки и так далее, и наша батарея накапливает некоторые плохие воспоминания. Эффект памяти силен для некоторых типов элементов, таких как батареи на никелевой основе. Другие типы, такие как литий-ионные, не страдают этой проблемой.
Другой аспект аккумуляторных батарей заключается в том, что химический состав, делающий их перезаряжаемыми, также означает, что они имеют более высокую тенденцию к саморазряду.Это когда внутренние реакции происходят внутри аккумуляторного элемента, даже когда электроды не подключены через внешнюю цепь. Это приводит к тому, что клетка со временем теряет часть своей химической энергии. Высокая скорость саморазряда серьезно ограничивает срок службы аккумуляторов — и приводит к их разрядке во время хранения.
Литий-ионные аккумуляторы в наших мобильных телефонах имеют довольно хорошую скорость саморазряда около 2–3 процентов в месяц, и наши свинцово-кислотные автомобильные аккумуляторы также довольно разумны — они, как правило, теряют 4–6 процентов. месяц.Никелевые батареи теряют около 10–15 процентов своего заряда в месяц, что не очень хорошо, если вы планируете хранить фонарик в течение всего сезона, когда он вам не нужен! Неперезаряжаемая щелочная батарея теряет около 2–3% своего заряда в год.
Напряжение, ток, мощность, емкость… в чем разница?
Все эти слова в основном описывают мощность батареи, не так ли? Ну вроде как.Но все они несколько разные.
Напряжение = сила, при которой реакция, приводящая в действие аккумулятор, проталкивает электроны через элемент. Это также известно как электрический потенциал и зависит от разницы потенциалов между реакциями, которые происходят на каждом из электродов, то есть от того, насколько сильно катод будет тянуть электроны (через цепь) от анода. Чем выше напряжение, тем больше работы может совершить то же количество электронов.
Ток = количество электронов, которые проходят через любую точку цепи в данный момент времени.Чем выше ток, тем больше работы он может выполнять при том же напряжении. Внутри ячейки ток можно также рассматривать как количество ионов, проходящих через электролит, умноженное на заряд этих ионов.
Мощность = напряжение x ток. Чем выше мощность, тем быстрее батарея может работать — это соотношение показывает, как напряжение и ток важны для определения того, для чего подходит батарея.
Емкость = мощность батареи как функция времени, которая используется для описания продолжительности времени, в течение которого батарея может обеспечивать питание устройства.Аккумулятор большой емкости сможет проработать более длительный период, прежде чем разрядится / разрядится. У некоторых батарей есть небольшая печальная особенность — если вы слишком быстро попытаетесь извлечь из них слишком много энергии, химические реакции не успеют поспеть, и емкость станет меньше! Итак, мы всегда должны быть осторожны, когда говорим о емкости аккумулятора, и помнить, для чего он будет использоваться.
Еще один популярный термин — «плотность энергии». Это количество энергии, которое устройство может удерживать на единицу объема, другими словами, сколько энергии вы получите за свои деньги с точки зрения мощности по сравнению сразмер. С батареей, как правило, чем выше плотность энергии, тем лучше, так как это означает, что батарея может быть меньше и компактнее, что всегда является плюсом, когда вам нужно заряжать то, что вы хотите держать в кармане. Для электромобилей это даже плюс — аккумулятор должен как-то влезать в машину!
Для некоторых приложений, таких как хранение электроэнергии на возобновляемых электростанциях, таких как ветряная или солнечная ферма, высокая плотность энергии не является большой проблемой, поскольку в них, скорее всего, будет достаточно места для хранения батарей.Основная цель такого использования — просто хранить как можно больше электроэнергии, как можно безопаснее и дешевле.
Почему так много типов?
Ряд материалов (раньше это были просто металлы) можно использовать в качестве электродов в батарее. За прошедшие годы было опробовано много-много различных комбинаций, но лишь немногие из них действительно прошли дистанцию.Но зачем вообще использовать разные комбинации металлов? Если у вас есть пара металлов, которые хорошо работают вместе в качестве электродов, зачем возиться с другими?
Различные материалы имеют разные электрохимические свойства, поэтому они дают разные результаты, когда вы соединяете их в аккумуляторном элементе. Например, некоторые комбинации будут производить высокое напряжение очень быстро, но затем быстро падают, не в состоянии поддерживать это напряжение в течение длительного времени. Это хорошо, если вам нужно произвести, скажем, внезапную вспышку света, такую как вспышка фотоаппарата.
Другие комбинации будут производить только тонкую струйку тока, но они будут поддерживать эту струю на века. Например, нам не нужен большой ток для питания детектора дыма, но мы хотим, чтобы наши детекторы дыма работали долгое время.
Еще одна причина для использования различных комбинаций металлов заключается в том, что часто два или более аккумуляторных элемента необходимо уложить в стопку для получения необходимого напряжения, и оказывается, что некоторые комбинации электродов складываются вместе намного удобнее, чем другие комбинации.Например, литий-железо-фосфатные батареи (тип литий-ионных аккумуляторов), используемые в электромобилях, складываются вместе для создания систем высокого напряжения (100 или даже более вольт), но вы никогда не сделаете этого с теми батареями NiCad Walkman, которые имеют горячий!
Наши различные потребности с течением времени привели к разработке огромного количества типов батарей. Чтобы узнать больше о них и о том, что ждет аккумулятор в будущем, ознакомьтесь с другими нашими темами о Nova.
Эта тема является частью нашей серии из четырех статей об аккумуляторах.Для дальнейшего чтения ознакомьтесь с типами аккумуляторов, литий-ионных аккумуляторов и аккумуляторов будущего.Как работают батарейки?
Как работают батарейки?Как работают батарейки?
Электричество, как вы, наверное, уже знаете, это поток электронов. через токопроводящую дорожку, как провод. Этот путь называется цепью .
Батареи состоят из трех частей: анода (-), катода (+), и электролит .Катод и анод (положительный и отрицательный стороны на обоих концах традиционной батареи) подключены к электрическому схема.
Химические реакции в батарее вызывают накопление электронов. на аноде. Это приводит к электрической разнице между анодом и катод. Вы можете думать об этой разнице как о нестабильном накоплении электроны. Электроны хотят перестроиться, чтобы избавиться от этой разницы.Но они делают это определенным образом. Электроны отталкиваются и пытаются уйти в место с меньшим количеством электронов.
В батарее единственное место, куда можно подойти, — это катод. Но электролит не позволяет электронам идти прямо от анода к катоду внутри батареи. Когда цепь замкнута (провод соединяет катод и анод) электроны смогут попасть на катод. На картинке выше электроны проходят по проводу, зажигая лампочку вдоль способ.Это один из способов описания того, как электрический потенциал вызывает появление электронов. протекать по контуру.
Однако эти электрохимические процессы изменяют химические вещества. в аноде и катоде, чтобы они перестали подавать электроны. Итак, есть ограниченное количество энергии, доступной в батарее.
Когда вы перезаряжаете аккумулятор, вы меняете направление потока электронов с помощью другого источника энергии, например солнечных батарей.В электрохимические процессы происходят в обратном порядке, и анод и катод восстанавливаются в исходное состояние и снова может обеспечить полную мощность.
Что есть батареи?
Что это энергия?
Что такое схема?
Что такое электрон?
Что такое поток электронов?
Что такое DS1 срок службы батареи?
Что значит электрически заряженный?
Как атомы заряжены?
Где энергия приходит и уходит?
Типы батарей / источников питания: принципы работы и преимущества
Батареи являются наиболее распространенным источником питания для базовых портативных устройств и крупномасштабных промышленных приложений.Батарею можно определить как; это комбинация одной или нескольких электрохимических ячеек, которые способны преобразовывать накопленную химическую энергию в электрическую.
Работа батареи:
Аккумулятор — это устройство, состоящее из различных гальванических элементов. Каждый гальванический элемент состоит из двух полуэлементов, соединенных последовательно проводящим электролитом, содержащим анионы и катионы. Одна полуячейка включает электролит и электрод, к которому перемещаются анионы, то есть анод или отрицательный электрод; другая полуячейка включает электролит и электрод, к которому движутся катионы, т.е.е. катод или положительный электрод.
В окислительно-восстановительной реакции, которая приводит в действие аккумулятор, происходит восстановление катионов на катоде, а окисление происходит до анионов на аноде. Электроды не касаются друг друга, а электрически связаны электролитом. В основном полуэлементы имеют разные электролиты. Учитывая все обстоятельства, каждая полуячейка заключена в контейнер, а сепаратор, пористый для ионов, но не большая часть электролитов, предотвращает смешивание.
Работа батареиКаждая половина ячейки имеет электродвижущую силу (ЭДС), определяемую ее способностью передавать электрический ток изнутри во внешнюю часть ячейки.Чистая ЭДС ячейки — это разница между ЭДС ее полуячеек. Таким образом, если электроды имеют ЭДС, другими словами, чистая ЭДС представляет собой разность восстановительных потенциалов полуреакций.
Как ухаживать за аккумулятором?
Чтобы поддерживать аккумулятор в хорошем состоянии, необходимо выравнивание заряда аккумулятора. Из-за старения все элементы заряжаются по-разному, некоторые элементы заряжаются очень быстро, а другие заряжаются постепенно. Выравнивание может быть выполнено путем небольшой перезарядки аккумулятора, чтобы позволить более слабым элементам также полностью зарядиться.Напряжение на клеммах полностью заряженной батареи составляет 12 В, автомобильная батарея показывает 13,8 В на клеммах, а 12-вольтовая трубчатая батарея — 14,8 В. Автомобильный аккумулятор должен быть надежно закреплен в автомобиле, чтобы избежать тряски. Батарею инвертора следует по возможности поставить на деревянную доску.
2 типа батарей
1) Первичные батареи:
Как видно из названия, эти батареи предназначены для одноразового использования. После того, как эти батареи используются, их нельзя перезарядить, так как устройства не могут быть легко восстановлены, и активные материалы могут не вернуться к своей первоначальной форме.Производители батарей не рекомендуют перезаряжать первичные элементы.
Некоторыми примерами одноразовых батареек являются обычные батарейки AA, AAA, которые мы используем в настенных часах, пультах дистанционного управления от телевизора и т. Д. Другое название этих батарей — одноразовые батарейки.
Типы батареи
2) Вторичные батареи:
Вторичные батареи также называются аккумуляторными. Эти батареи можно использовать и заряжать одновременно. Обычно они собираются с активными материалами, причем активный элемент находится в разряженном состоянии.Перезаряжаемые батареи заряжаются с помощью электрического тока, который обращает вспять химические реакции, происходящие во время разряда. Зарядные устройства — это устройства, обеспечивающие необходимый ток.
Примерами таких аккумуляторных батарей являются батареи, используемые в мобильных телефонах, MP3-плеерах и т. Д. В таких устройствах, как слуховые аппараты и наручные часы, используются миниатюрные элементы, а в таких местах, как телефонные станции или компьютерные центры обработки данных, используются более крупные батареи.
Вторичные батареиТипы вторичных (аккумуляторных) батарей:
SMF, свинцово-кислотные, Li и Nicd
SMF Батарея:
SMF — это герметичная необслуживаемая батарея , разработанная для обеспечения надежного, стабильного и не требующего обслуживания питания для ИБП.Эти батареи могут подвергаться глубокому разряду и минимальному техническому обслуживанию в сельской местности и в районах с дефицитом электроэнергии. Эти батареи доступны от 12 В.
В современном информативном мире нельзя упускать из виду требование, чтобы аккумуляторные системы были разработаны для восстановления важных квалифицированных данных и информации и запуска основных контрольно-измерительных приборов в течение желаемой продолжительности. Батареи необходимы для мгновенной подачи энергии. Ненадежные и некачественные батареи могут привести к потере данных и отключению оборудования, что может стоить компаниям значительных финансовых потерь.Следовательно, сегменты ИБП требуют использования надежной и проверенной аккумуляторной системы.
Батарея SMFЛитиевая (Li) Батарея:
Все мы используем его в портативных устройствах, таких как сотовый телефон, портативный компьютер или электроинструмент. Литиевая батарея была одним из величайших достижений портативной энергетики за последнее десятилетие; Благодаря использованию литиевых батарей мы смогли перейти с черно-белых мобильных телефонов на цветные с дополнительными функциями, такими как GPS, оповещения по электронной почте и т. д.Это устройства с потенциалом высокой плотности энергии для более высоких мощностей. И относительно невысокий саморазряд аккумуляторов. Также специальные элементы могут обеспечивать очень высокий ток для таких приложений, как электроинструменты.
Литий-ионный аккумуляторНикель-кадмиевый (Nicd) аккумулятор:
Никель-кадмиевые батареи имеют то преимущество, что их можно перезаряжать много раз, они обладают относительно постоянным потенциалом во время разряда и имеют большую электрическую и физическую стойкость. В этой батарее используется оксид никеля для катода, соединение кадмия для анода и раствор гидроксида калия в качестве электролита.
Когда аккумулятор заряжается, химический состав катода изменяется, и гидроксид никеля изменяется на NIOOH. В аноде образование ионов кадмия происходит из гидроксида кадмия. Когда аккумулятор разряжен, кадмий реагирует с NiOOH с образованием гидроксида никеля и гидроксида кадмия.
Cd + 2h3O + 2NiOOH -> 2Ni (OH) 2 + Cd (OH) 2
Свинцово-кислотная батарея:
Свинцово-кислотные батареишироко используются в автомобилях, инверторах, системах резервного питания и т. Д.В отличие от трубчатых и необслуживаемых батарей, свинцово-кислотные батареи требуют надлежащего ухода и обслуживания для продления срока их службы. Свинцово-кислотная батарея состоит из ряда пластин, погруженных в раствор серной кислоты. Пластины имеют решетки, на которые крепится активный материал. Пластины делятся на положительные и отрицательные. Положительные пластины содержат чистый свинец в качестве активного материала, в то время как оксид свинца прикреплен к отрицательным пластинам.
Свинцово-кислотная батареяПолностью заряженная батарея может разрядить ток при подключении к нагрузке.В процессе разряда серная кислота соединяется с активными материалами на положительной и отрицательной пластинах, что приводит к образованию сульфата свинца. Вода — самый важный шаг в обслуживании свинцово-кислотной батареи. Периодичность подачи воды зависит от использования, способа зарядки и рабочей температуры. Во время процесса атомы водорода серной кислоты реагируют с кислородом с образованием воды.
Это приводит к высвобождению электронов из положительных пластин, которые будут приняты отрицательными пластинами.Это приводит к образованию электрического потенциала на батарее. Электролит в свинцово-кислотной батарее представляет собой смесь серной кислоты и воды, имеющую удельный вес. Удельный вес — это вес кислотно-водной смеси по сравнению с равным объемом воды. Удельный вес чистой воды, свободной от ионов, составляет 1.
.Свинцово-кислотные батареи обеспечивают лучшее соотношение мощности и энергии на киловатт-час; имеют самый продолжительный жизненный цикл и большое экологическое преимущество, поскольку они перерабатываются с чрезвычайно высокой скоростью.Никакая другая химия не может коснуться инфраструктуры, которая существует для сбора, транспортировки и переработки свинцово-кислотных аккумуляторов.
Наряду с этой статьей обсуждается литий-ионный аккумулятор, его достоинства и недостатки.
Работа литий-ионной батареи
Литий-ионные батареисейчас популярны в большинстве портативных электронных устройств, таких как мобильные телефоны, ноутбуки, цифровые фотоаппараты и т. Д., Благодаря их длительной энергоэффективности. Это самые популярные аккумуляторные батареи с такими преимуществами, как лучшая плотность энергии, незначительные потери заряда и отсутствие эффекта памяти.Литий-ионный аккумулятор использует ионы лития в качестве носителей заряда, которые перемещаются от отрицательного электрода к положительному во время разряда и обратно при зарядке. Во время зарядки внешний ток от зарядного устройства вызывает перенапряжение, чем в аккумуляторе. Это заставляет ток проходить в обратном направлении от положительного электрода к отрицательному, где ионы лития внедряются в пористый электродный материал в результате процесса, называемого интеркаляцией. Ионы лития проходят через неводный электролит и разделительную диафрагму.Материал электрода — интеркалированное соединение лития.
Отрицательный электрод литий-ионной батареи состоит из углерода, а положительный электрод — из оксида металла. Чаще всего для отрицательного электрода используется графит, а для положительного электрода — оксид лития-кобальта, литий-ионный фосфат или оксид лития-марганца. Литиевая соль в органическом растворителе используется в качестве электролита. Электролит обычно представляет собой смесь органических карбонатов, таких как этиленкарбонат или диэтилкарбонат, содержащих ионы лития.В электролите используются анионные соли, такие как гексафторфосфат лития, моногидрат гексафторарсената лития, перхлорат лития, гексафторборат лития и т. Д. В зависимости от используемой соли напряжение, емкость и срок службы батареи различаются. Чистый литий бурно реагирует с водой с образованием гидроксида лития и ионов водорода. Таким образом, в качестве электролита используется неводный органический растворитель. Электрохимическая роль заряда электродов между анодом и катодом зависит от направления тока.
Li-Ion Battery ReactionВ литий-ионной батарее оба электрода могут принимать и выделять ионы лития. Во время процесса интеркаляции ионы лития перемещаются в электрод. Во время обратного процесса, называемого деинтеркаляцией, ионы лития возвращаются. Во время разряда положительные ионы лития извлекаются из отрицательных электродов и вставляются в положительный электрод. В процессе зарядки происходит обратное движение ионов лития.
Преимущества литий-ионной батареи:
Литий-ионные батареипревосходят никель-кадмиевые батареи и другие вторичные батареи.Некоторые из преимуществ
- Легкий вес по сравнению с другими батареями аналогичного размера
- Доступны разные формы, включая плоскую
- Высокое напряжение холостого хода, увеличивающее передачу мощности при низком токе
- Отсутствие эффекта памяти.
- Очень низкая скорость саморазряда 5-10% в месяц. Саморазряд составляет около 30% у никель-кадмиевых и никель-металлгидридных аккумуляторов.
- Экологичный аккумулятор без свободного металлического лития
Но наряду с достоинствами, как и у других аккумуляторов, у Li-Ion есть и недостатки.
Недостатки литий-ионного аккумулятора:
- Отложения внутри электролита со временем будут препятствовать прохождению заряда. Это увеличивает внутреннее сопротивление батареи, и способность элемента передавать ток постепенно уменьшается.
- Высокая зарядка и высокая температура могут привести к потере емкости
- При перегреве литий-ионная аккумуляторная батарея может терять тепло и разрушаться.
- Глубокая разрядка может привести к короткому замыканию литий-ионного аккумулятора. Поэтому, чтобы предотвратить это, некоторые производители имеют внутреннюю схему отключения, которая отключает аккумулятор, когда его напряжение превышает безопасный уровень от 3 до 4.2 вольта. В этом случае, когда аккумулятор не используется в течение длительного времени, внутренняя схема будет потреблять энергию и разряжать аккумулятор ниже напряжения отключения. Так что для зарядки таких аккумуляторов обычные зарядные устройства не пригодятся.
DOE объясняет … Батареи | Министерство энергетики
Аккумуляторы и аналогичные устройства принимают, хранят и отпускают электроэнергию по запросу. В батареях используется химия в форме химического потенциала для хранения энергии, как и во многих других повседневных источниках энергии.Например, бревна хранят энергию в своих химических связях, пока при горении энергия не преобразуется в тепло. Бензин — это запасенная химическая потенциальная энергия, пока она не преобразуется в механическую энергию в двигателе автомобиля. Точно так же, чтобы батареи работали, электричество должно быть преобразовано в форму химического потенциала, прежде чем оно может быть легко сохранено. Батареи состоят из двух электрических клемм, называемых катодом и анодом, разделенных химическим материалом, называемым электролитом. Чтобы принимать и высвобождать энергию, батарея подключается к внешней цепи.Электроны движутся по цепи, в то время как одновременно ионы (атомы или молекулы с электрическим зарядом) движутся через электролит. В перезаряжаемой батарее электроны и ионы могут двигаться в любом направлении через цепь и электролит. Когда электроны движутся от катода к аноду, они увеличивают химическую потенциальную энергию, таким образом заряжая аккумулятор; когда они движутся в другом направлении, они преобразуют эту химическую потенциальную энергию в электрическую цепь и разряжают батарею.Во время зарядки или разрядки противоположно заряженные ионы перемещаются внутри батареи через электролит, чтобы уравновесить заряд электронов, проходящих через внешнюю цепь, и создать устойчивую перезаряжаемую систему. После зарядки аккумулятор может быть отключен от цепи для хранения химической потенциальной энергии для последующего использования в качестве электричества.
Батареи были изобретены в 1800 году, но их химические процессы сложны. Ученые используют новые инструменты, чтобы лучше понять электрические и химические процессы в батареях, чтобы создать новое поколение высокоэффективных аккумуляторов электроэнергии.Например, они разрабатывают улучшенные материалы для анодов, катодов и электролитов в батареях. Ученые изучают процессы в аккумуляторных батареях, потому что они не полностью меняются, когда батарея заряжается и разряжается. Со временем отсутствие полной замены может изменить химический состав и структуру материалов батареи, что может снизить производительность и безопасность батареи.
Департамент науки и хранения электроэнергии Министерства энергетики США
Исследования, проведенные при поддержке Управления науки Министерства энергетики США и Управления фундаментальных энергетических наук (BES), привели к значительным улучшениям в хранении электроэнергии.Но мы все еще далеки от комплексных решений для хранения энергии следующего поколения с использованием совершенно новых материалов, которые могут значительно увеличить количество энергии, которое может хранить батарея. Это хранилище имеет решающее значение для интеграции возобновляемых источников энергии в нашу систему электроснабжения. Поскольку усовершенствование аккумуляторных технологий имеет важное значение для повсеместного использования подключаемых к электросети электромобилей, хранение также является ключом к уменьшению нашей зависимости от нефти при транспортировке.
BES поддерживает исследования отдельных ученых и в многопрофильных центрах.Самый крупный центр — Объединенный центр исследований в области накопления энергии (JCESR), центр энергетических инноваций Министерства энергетики США. Этот центр изучает электрохимические материалы и явления на атомном и молекулярном уровне и использует компьютеры для разработки новых материалов. Эти новые знания позволят ученым разработать более безопасные накопители энергии, которые служат дольше, заряжаются быстрее и обладают большей емкостью. По мере того как ученые, поддерживаемые программой BES, достигают новых успехов в науке об аккумуляторах, эти достижения используются прикладными исследователями и промышленностью для продвижения приложений в области транспорта, электросетей, связи и безопасности.
Факты о хранении электрической энергии
- Нобелевская премия по химии 2019 года была присуждена совместно Джону Б. Гуденафу, М. Стэнли Уиттингему и Акире Йошино «за разработку литий-ионных батарей».
- Компания Electrolyte Genome в JCESR создала вычислительную базу данных, содержащую более 26 000 молекул, которую можно использовать для расчета основных свойств электролита для новых усовершенствованных аккумуляторов.
Ресурсы и связанные термины
Научные термины могут сбивать с толку.DOE Explains предлагает простые объяснения ключевых слов и концепций фундаментальной науки. В нем также описывается, как эти концепции применяются к работе, которую проводит Управление науки Министерства энергетики США, поскольку это помогает Соединенным Штатам преуспеть в исследованиях по всему научному спектру.
Как работают батареи Принцип работы, хранение и старение_Greenway battery
Батарея — это устройство, которое накапливает энергию в форме химических веществ и при необходимости преобразует ее в электрическую.А это обычные батарейки — те, что имеют хорошо знакомую цилиндрическую форму. Нет батареи, которая хранит электрическую энергию, и каждая батарея хранит энергию в какой-либо другой форме. Чтобы узнать больше о том, как работают батареи, мы рекомендуем вам продолжить чтение, чтобы узнать об этом и узнать все, что вам нужно знать о работе батареи.
Каков принцип работы аккумулятора?
+ Когда два разных металла, называемых электродами, помещаются в разбавленный электролит, в электродах происходят реакции окисления и восстановления, в зависимости от электронного контакта металла электродов.Из-за реакции окисления один электрод получает отрицательный заряд, называемый катодом. Другой электрод получает положительный заряд, называемый анодом, из-за реакции восстановления. Катод образует отрицательную клемму, а анод — положительную клемму элемента или батареи.
Чтобы понять фундаментальный принцип батареи, вам необходимо понять основную концепцию сродства электронов. Когда два, в отличие от металлов, помещаются в электролит, между этими металлами возникает разность потенциалов.
Обнаружено, что когда в воду добавляют определенные соединения, они растворяются и генерируют положительные и отрицательные ионы. Этот вид соединения известен как электролит. Энергия, возникающая при принятии электрона нейтральным атомом, называется сродством к электрону. Если два разных типа металлов поместить в один и тот же раствор электролита, то один будет получать электроны, а другой — высвободить электроны. И какой металл получит электроны, а какой потеряет, зависит от сродства к электрону.Металл с более низким сродством приобретает электроны у -ve-ионов раствора электролита.
С другой стороны, металл с высоким сродством к электрону в конечном итоге будет высвобождать электроны. Следовательно, будет ключевое различие в концентрации электронов между этими двумя металлами. Эта разница приводит к образованию разницы электрических потенциалов между металлами. Эту разность или ЭДС можно использовать как источник напряжения в любой электрической цепи. Это общий принцип работы аккумулятора.
Как аккумулятор накапливает энергию?
Существует два основных типа химических аккумуляторных батарей: аккумуляторные или вторичные, первичные или неперезаряжаемые. Что касается хранения энергии или разряда электричества, они идентичны. Это просто вопрос, допускают ли задействованные химические процедуры многократную зарядку, а также разрядку.
Все электрохимические ячейки имеют два электрода. Область между электродами заполнена электролитом — ионной жидкостью, проводящей электричество.Электрод — анод — позволяет электронам выходить из него. Другой — катод — принимает их. Энергия хранится в специальных соединениях, из которых состоят анод, катод и электролит, например в цинке, меди и SO4.
Анод подвергается реакции окисления: во время разряда два или более иона объединяются с анодом, образуя соединение, а также высвобождают 1 или более электронов. Катод подвергается реакции восстановления, в которой материал, из которого изготовлен катод, образует соединения с ионами и свободными электронами.
Как умирает аккумулятор?
Когда активное вещество в пластинах не может выдерживать поток разряда, батарея «умирает». Как правило, автомобильный (или ранний) аккумулятор «стареет» по мере того, как активный материал положительной пластины отслаивается (или отслаивается) из-за нормального расширения и сжатия, которое происходит во время циклов разрядки и зарядки. Это приводит к тому, что пластина теряет емкость, и коричневый осадок, называемый шламом или «грязью», накапливается на дне корпуса, а также замыкает пластину элемента.Это как можно быстрее повредит аккумулятор.
В жаркую погоду дополнительными причинами отказа являются положительный рост сетки, положительное повреждение металла сетки, отрицательная усадка сетки, коробление пластин или потеря воды. Глубокие разряды, вибрация, нагрев, быстрая зарядка и избыточная зарядка — все это стимулирует процесс «старения». Около 50% преждевременных отказов автомобильных аккумуляторов вызваны недостаточным обслуживанием, испарением из-за высокой геотермальной температуры или потерей воды для нормальной подзарядки из-за перезарядки.Положительный рост сети и недозаряд, вызванный сульфатированием, могут привести к преждевременным сбоям.
Срок службы батареи зависит от ее химического возраста, который превышает время после сборки батареи. Химический возраст батареи определяется сложным сочетанием нескольких факторов, включая температурный режим и режим зарядки. Все аккумуляторные батареи годны к использованию и не обладают химической эффективностью с возрастом. По мере химического старения литий-ионных аккумуляторов количество удерживаемого ими заряда уменьшается, срок службы аккумулятора уменьшается, а максимальная производительность снижается.
Заключение
Вот и все. Здесь мы рассмотрели основную идею работы батарей. Энергия хранится в специальных соединениях, из которых состоят анод, катод и электролит. Аккумулятор становится заряженным во время зарядки или сборки устройства. Во время разряда химическое вещество на аноде высвобождает электроны, а ионы в электролите подвергаются реакции окисления. Многие электрохимические и термические процессы происходят одновременно, и даже самые практичные комбинации элементов, упакованные в виде батарей, не могут полностью отобразить все процессы.Таким образом, приближение основных реакций является лишь кратким описанием того, что происходит на самом деле, но оно также помогает объяснить основной принцип работы батареи.
литий-ионный аккумулятор аккумулятор для электровелосипеда литиевая батарея
Принцип работы литий-ионного аккумулятора — E-Lyte Innovations
Принцип работы литий-ионного аккумулятора — E-Lyte InnovationsЛитий-ионные батареи относятся к группе батарей, вырабатывающих электрическую энергию путем преобразования химической энергии посредством окислительно-восстановительных реакций на активных материалах, т.е.е. отрицательный (анод) и положительный электрод (катод) в одной или нескольких электрически связанных электрохимических ячейках. Литий-ионные батареи можно разделить на первичные (неперезаряжаемые) и вторичные (перезаряжаемые) батареи, в зависимости от того, перезаряжаются ли они под действием электрического тока.
В обычных литий-ионных батареях Li + -ионы перемещаются между положительным электродом (обычно слоистым материалом оксида переходного металла) и отрицательным электродом на основе графита в соответствии с принципом «кресла-качалки» (см.видео).
Термин «разряд» используется для обозначения процесса, при котором аккумулятор подает электрическую энергию на внешнюю нагрузку. Электролит в этой системе содержит дополнительные ионы Li + для обеспечения быстрого переноса ионного заряда внутри элемента.
Помимо ионной проводимости, электролит выполняет другие важные функции:Поддержка образования эффективных межфазных фаз (например, межфазной границы твердого электролита, SEI или межфазной поверхности катодного электролита, CEI), которые:
- включить аккумулятор для работы
- хорошо Li + -ион проводящий (оцените!)
- защищают от дальнейшего разложения электролита
Способствовать безопасности клеток — быть инертным по отношению к другим материалам, таким как:
- Сепаратор
- Токосъемники
- Электропроводящие добавки, связующие
- Оболочка ячейки
Шаг 1 — Исходное состояние (состояние заряда (SOC) 0%)
В разряженном состоянии ионы Li + находятся в материале положительного электрода.Таким образом, положительный электрод является источником ионов Li + , необходимых для преобразования электрической энергии в химическую энергию. Чтобы позволить ионам Li + мигрировать с положительного электрода на отрицательный, электролит также обогащен ионами Li + .
Шаг 2 — Формирование SEI и CEI
В самом начале первого процесса зарядки электроны мигрируют из материала положительного электрода (окисление) через внешний проводник в материал отрицательного электрода (восстановление).Чтобы гарантировать нейтральность заряда, ионы Li + деинтеркалируются из материала положительного электрода в электролит и мигрируют через электролит в материал отрицательного электрода для последующего хранения. В результате этих реакций на границах раздела между электролитом / поверхностью отрицательного электрода и электролитом / поверхностью положительного электрода, соответственно, образуются граничные фазы, так называемые SEI и CEI. Эти промежуточные фазы образуются из нерастворимых электрохимически индуцированных продуктов разложения компонентов электролита и ионов Li + , происходящих от положительного электрода, и обеспечивают обратимое циклическое переключение батареи.После образования SEI и CEI дополнительные ионы Li + деинтеркалируются из материала положительного электрода в электролит и мигрируют через него в материал отрицательного электрода, чтобы затем встраиваться в последний.
Шаг 3 — Электродные реакции
После образования SEI и CEI, ионы Li + деинтеркалируют из материала положительного электрода в электролит и мигрируют через него в материал отрицательного электрода, чтобы затем встраиваться в последний.
Положительный электрод:
Li M O 2 → Li (1- x ) M O 2 + x · e — + x · Li +
Отрицательный электрод:
C 6 + x · e — + x · Li + → Li x C 6
Общая реакция клетки:
C 6 + Li M O 2 → Li x C 6 + Li (1- x ) MO 2
Шаг 5 — Выписка
При разряде происходят обратные реакции.Электродные реакции:
Положительный электрод = «катод» (восстановление)
Li (1- x ) M O 2 + x · e — + x · Li + → Li M O 2
Отрицательный электрод = «анод» (окисление)
Li x C 6 → C 6 + x · e — + x · Li +
Шаг 6 — Принцип кресла-качалки
После разряда (SOC 0%) ионы Li + повторно сохраняются в материале положительного электрода, из которого они изначально были получены.Возвратно-поступательное движение Li + -ions напоминает движение кресла-качалки, поэтому этот принцип получил название «принцип кресла-качалки».
В частности, первый цикл (заряд и разряд) связан с необратимой потерей ионов Li + в SEI и CEI, а также в материале отрицательного электрода. В результате меньшее количество ионов Li + теперь может храниться в отрицательном электроде в следующем цикле зарядки, что приводит к уменьшению емкости аккумулятора.
В литий-ионной батарее происходят различные процессы старения, которые снижают производительность батареи в течение периода использования и сильно зависят от химического состава элемента и предполагаемого использования батареи. Особенно правильный выбор электролита имеет огромное влияние на эти механизмы старения и еще раз подчеркивает важность индивидуальных электролитов.
Для оптимизации литий-ионных батарей в отношении удельной энергии и плотности энергии, срока службы и безопасности было приложено много усилий для дальнейшего расширения возможностей применения LIB.В частности, растущие потребности в литий-ионных батареях с высокой удельной энергией и плотностью энергии, особенно для автомобильных приложений, увеличивают исследовательские усилия во всем мире. Плотность энергии и удельная энергия батарей по определению — это количество энергии, хранящейся в данной системе на единицу объема и на единицу массы, соответственно. Произведение удельной емкости и среднего напряжения разряда дает удельную энергию, и это соотношение находит выражение в уравнении 1:
.E = C · U (1)
Согласно уравнению 1 кажется разумным, что большая часть текущих исследований сосредоточена на новых материалах положительного электрода с более высокими рабочими напряжениями (высоковольтный подход) и / или увеличенной удельной емкостью (подход с высокой емкостью).Материалы высоковольтных катодов сильно ограничены узким окном электрохимической стабильности современных электролитов на основе карбонатов (≈1,0 — 4,4 В по сравнению с Li / Li + ) и усиливают конструкцию искробезопасных электролитов. электролиты или подходящие добавки к электролиту для высоковольтных литий-ионных батарей.
Мы используем файлы cookie на нашем веб-сайте. Некоторые из них очень важны, а другие помогают нам улучшить этот веб-сайт и улучшить ваш опыт.
Принять все
Сохранить
Принимать только необходимые файлы cookie
Индивидуальные настройки конфиденциальности
Подробная информация о файлах cookie Политика конфиденциальности Отпечаток
Предпочтение конфиденциальностиЗдесь вы найдете обзор всех используемых файлов cookie.Вы можете дать свое согласие на использование целых категорий или отобразить дополнительную информацию и выбрать определенные файлы cookie.
| Имя | Borlabs Cookie |
|---|---|
| Провайдер | Владелец этого сайта |
| Назначение | Сохраняет предпочтения посетителей, выбранные в поле Cookie Borlabs Cookie. |
| Имя файла cookie | Borlabs-печенье |
| Срок действия куки | 1 год |
Battery 101: как работает автомобильный аккумулятор?
Вашему автомобилю, как и пульту дистанционного управления от телевизора или необычной электрической зубной щетке, для работы необходим аккумулятор.Когда он умирает, ваша машина не заводится, в результате чего вы либо застрянете, либо застрянете дома. Вы знаете, что автомобильный аккумулятор важен, но действительно ли вы понимаете, как он питает ваш двигатель, фары и радио? Следуйте инструкциям, пока мы разберем сложности с аккумулятором и объясним, как работают автомобильные аккумуляторы! Если знания — это сила, вы будете в отличной форме.
Что такое аккумулятор?
Прежде чем углубляться в детали автомобильных аккумуляторов, давайте посмотрим, как аккумуляторы в целом работают.По словам сотрудников НАСА, аккумулятор — это «устройство, преобразующее химическую энергию в электричество». Батареи состоят из ячеек. Эти клетки и содержат настоящую энергию. Они накапливают химическую энергию и по команде преобразуют ее в электрическую. Это то, что питает ваши устройства, от пульта телевизора до электрической зубной щетки.
Как работают автомобильные аккумуляторы?
Большинство автомобильных аккумуляторов основываются на свинцово-кислотной химической реакции, которая приводит в движение и прорезание канавок.Эти батареи относятся к категории «SLI». SLI означает «запуск, освещение и зажигание». Этот тип батареи обеспечивает короткие всплески энергии для питания ваших фонарей, аксессуаров и двигателя. Как только аккумулятор пробуждает двигатель к жизни, питание для автомобиля подается от генератора. Большинство автомобилей поставляются с заводской стандартной батареей SLI. Узнайте больше о других типах автомобильных аккумуляторов.
Как работают автомобильные аккумуляторы
Нужен ли мне новый автомобильный аккумулятор?
Вы могли бы! Несмотря на то, что свинцово-кислотные батареи чрезвычайно надежны, несмотря на перепады температур, движение и стесненные условия под вашим капотом, типичный аккумулятор прослужит всего около трех-пяти лет.
